
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:期中题 题型:填空题
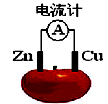
查看答案和解析>>
科目:高中化学 来源:陕西省模拟题 题型:填空题
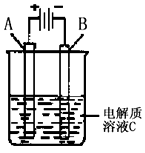
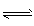 2CO2(g)+4H2O(g),试写出该条件下反应的平衡常数(K)___________ ; 在电脑的使用过程中,电池的温度往往因为各种原因会升高,试判断温度升高时该反应的平衡常数(K)____________(填增大、减小、不变),其反应的正反应速率 ___________(填增大、减小、不变);温度升高_________(填有利或不利于)电池将化学能转化为电能。
2CO2(g)+4H2O(g),试写出该条件下反应的平衡常数(K)___________ ; 在电脑的使用过程中,电池的温度往往因为各种原因会升高,试判断温度升高时该反应的平衡常数(K)____________(填增大、减小、不变),其反应的正反应速率 ___________(填增大、减小、不变);温度升高_________(填有利或不利于)电池将化学能转化为电能。 
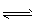 CO2(g)+H2(g)。 CO的转化率随时间变化关系如图,回答下列问题:
CO2(g)+H2(g)。 CO的转化率随时间变化关系如图,回答下列问题: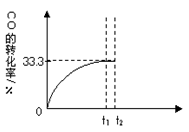
查看答案和解析>>
科目:高中化学 来源:山东省模拟题 题型:填空题
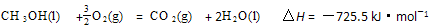
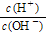 = 1×10- 6 ,则该溶液的pH为____,溶液中的溶质电离出的阳离子浓度约为_________;将 pH = 4的盐酸溶液V1 L与 0.01 mol·L-1 氨水V2 L混合,若混合溶液pH = 7,则V1 和V2 的关系为:V1________ V2 (填“>”、“<”或“=”)。
= 1×10- 6 ,则该溶液的pH为____,溶液中的溶质电离出的阳离子浓度约为_________;将 pH = 4的盐酸溶液V1 L与 0.01 mol·L-1 氨水V2 L混合,若混合溶液pH = 7,则V1 和V2 的关系为:V1________ V2 (填“>”、“<”或“=”)。查看答案和解析>>
科目:高中化学 来源:四川省模拟题 题型:填空题




查看答案和解析>>
科目:高中化学 来源:期末题 题型:单选题
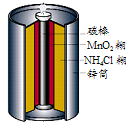
查看答案和解析>>
科目:高中化学 来源:期中题 题型:单选题
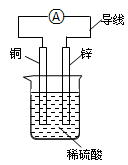
查看答案和解析>>
科目:高中化学 来源:广东省模拟题 题型:单选题
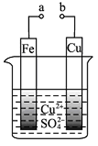
查看答案和解析>>
科目:高中化学 来源:0127 会考题 题型:单选题
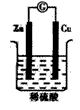
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com