
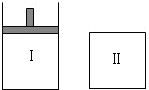
 ��ͼ�����Ǻ�ѹ�ܱ����������Ǻ����ܱ�����������������ͬʱ���ڢ��зֱ����2mol X��2mol Y����ʼʱ���������ΪV L���������·�Ӧ���ﵽƽ�⣨X��Y״̬δ֪����2X������+Y������?aZ��g������ʱ����X��Y��Z�����ʵ���֮��Ϊ1��3��2��������˵��һ����ȷ���ǣ�������
��ͼ�����Ǻ�ѹ�ܱ����������Ǻ����ܱ�����������������ͬʱ���ڢ��зֱ����2mol X��2mol Y����ʼʱ���������ΪV L���������·�Ӧ���ﵽƽ�⣨X��Y״̬δ֪����2X������+Y������?aZ��g������ʱ����X��Y��Z�����ʵ���֮��Ϊ1��3��2��������˵��һ����ȷ���ǣ�������| A����X��Y��Ϊ��̬����ƽ��ʱ����ƽ��Ħ���������� |
| B����X��Y����Ϊ��̬����ƽ��ʱ����ƽ��Ħ���������� |
| C����XΪ��̬��YΪ��̬������д���ʼ��ƽ������ʱ����ͬ |
| D��ƽ��ʱ�����������С��V L |
| 2-x |
| 2-0.5x |
| 1 |
| 3 |
| 2-0.16 |
| 0.08a |
| 1 |
| 2 |
| 2-x |
| 2-0.5x |
| 1 |
| 3 |
| 2-0.16 |
| 0.08a |
| 1 |
| 2 |
| m |
| n |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��NaAlO2��Һ��ͨ�������CO2��2AlO2-+CO2+3H2O=2Al��OH��3��+CO32- |
| B����ϡFe��NO3��2��NaBr�����Һ�еμ�ϡ����6Br-+8H++2NO3-=3Br2+2NO��+4H2O |
| C��Na2S��Һ�еμ�NaClO��Һ��S2-+ClO-+H2O=S��+Cl-+2OH- |
| D��˫��ˮʹ����KMnO4��Һ��ɫ2MnO4-+5H2O2=2Mn2++5O2��+6OH-+2H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���ٺ͢� | B���ں͢� |
| C���ۺ͢� | D���ܺ͢� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��θ��ƽ[��Ҫ�ɷ���Al��OH��3] |
| B���մ���Ҫ�ɷ���Na2CO3�� |
| C��С�մ���Ҫ�ɷ���NaHCO3�� |
| D��̼�ᱵ��ĩ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| A��ͼa����������һ��ʱ����Ӧ�������¶ȱ仯��ͼ������Ӧ��H��0 |
| B��ͼb���������������½�����ƽ�����ͼ������a��ʹ�ô��������� |
| C��ͼc��һ�������£�����һ����A������������Bʱ��ͼ��ѹǿp1��p2 |
| D��ͼd����ƽ����ϵ����Һ����������KCl�����ѧ��Ӧ������ʱ��仯��ͼ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��H+��CO32- |
| B��HCO3-��HSO4- |
| C��Na+��HCO3-��H+ |
| D��HCO3-��H+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Һ̬HCl�����磬����HCl�Ƿǵ���� |
| B��NH3��ˮ��Һ�ܹ����磬����NH3�ǵ���� |
| C��ͭ˿�ܵ��磬��ͭ˿�ǵ��ʣ��Ȳ��ǵ����Ҳ���Ƿǵ���� |
| D�������ᱵ����ˮ�в��ܵ��磬�������ᱵ���ǵ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����ȡ1.92gNaOH������480mLˮ |
| B����ȡ1.92gNaOH�����500mL��Һ |
| C����ȡ2.0gNaOH�����500mL��Һ |
| D����ȡ2.0gNaOH������500mLˮ |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com