
�����ڹ�ũҵ����������ҪӦ�á�
24�� ��ԭ�ӵ������ĵ����Ų�ʽ��______________����ԭ�Ӻ����_______�ֲ�ͬ�����ĵ��ӡ�
25������ͼ��ʾ����NaOH�����ϵμ���Ũ��ˮ��Ѹ�ٸ��ϸǣ��۲�����

��Ũ����Һ���Ϸ�û����������һ��ʱ���Ũ�����Һ�����а�ɫ���壬�ù��������
��FeSO4Һ�����ȳ��ֻ���ɫ��������һ��ʱ����ɺ��ɫ�������ķ�Ӧ����
Fe2+ + 2NH3��H2O �� Fe(OH)2��+ 2NH4+ �� _________ ������ѧ����ʽ��
26���������ѷ���Ŀǰ����NH3��ˮ����Ⱦ����Ҫ��������һ�������£���ˮ���м�������NaOH��ʹNH3���ѳ���������ƽ���ƶ�ԭ��������ԭ�� ��
27�������������£���������ˮ�зֽ�����İ��ܹ��������������������ᣨHNO2������Ӧ�Ļ�ѧ����ʽΪ ������Ӧ����0.3 mol���ӷ���ת��ʱ�����������������Ϊ g��С���������λ��Ч���֣���
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
X��Y��Z��Q��R�����ֶ�����Ԫ��,ԭ��������������X��Y��Ԫ����������������֮�;�Ϊ0��Q��Xͬ���壻Z��R�ֱ��ǵؿ��к�����ߵķǽ���Ԫ�غͽ���Ԫ�ء���ش���������:
(1)����Ԫ��ԭ�Ӱ뾶�ɴ�С��˳����(дԪ�ط���)������������������
(2)������ijЩԪ����ɵĻ�����A��B��C��D������ת����ϵ:A B����ˮ��Һ�н��У�������,C������ˮ�����Ե����壬D�ǵ���ɫ���塣д��C�Ľṹʽ:����������D�ĵ���ʽ:����������
B����ˮ��Һ�н��У�������,C������ˮ�����Ե����壬D�ǵ���ɫ���塣д��C�Ľṹʽ:����������D�ĵ���ʽ:����������
�����A��B��������Ԫ�����,BΪ���Բ������A�Ļ�ѧʽΪ����������Aת��ΪB�����ӷ���ʽΪ��������������������������������������
�����A������Ԫ����ɣ�B������Ԫ����ɣ�A��B��Һ���Լ��ԡ������ӷ���ʽ��ʾA��Һ�Լ��Ե�ԭ�����������������������������������ӷ���ʽ��ʾ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�ں���ʱ��һ�̶��ݻ��������ڷ������·�Ӧ��2NH3 (g)  N2 (g)+3H2 (g)����ƽ�������������ͨ��һ������NH3(g)�����´ﵽƽ������һ��ƽ��ʱ��ȣ�NH3���������( )
N2 (g)+3H2 (g)����ƽ�������������ͨ��һ������NH3(g)�����´ﵽƽ������һ��ƽ��ʱ��ȣ�NH3���������( )
A������ B������ C����С D�����ж�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
t ��ʱ�������������ܱ������з�����Ӧ��X(g)+3Y(g) 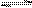 2Z(g)��������ڲ�ͬʱ�̵�Ũ�����±���
2Z(g)��������ڲ�ͬʱ�̵�Ũ�����±���
| ���� | X | Y | Z |
| ��ʼŨ��/mol��L-1 | 0.1 | 0.2 | 0 |
| 2 minĩŨ��/mol��L-1 | 0.08 | a | b |
| ƽ��Ũ��/mol��L-1 | 0.05 | 0.05 | 0.1 |
����˵����ȷ����
A��ƽ��ʱ��X��ת����Ϊ20%
B��t ��ʱ���÷�Ӧ��ƽ�ⳣ��Ϊ40
C������ƽ������ϵѹǿ�� v������v����С��ƽ��������Ӧ�����ƶ�
D��ǰ2 min�ڣ���Y�ı仯����ʾ��ƽ����Ӧ����v(Y) = 0.03 mol��L-1��min-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��BaCl2��Һ��ͨ�������������Һ��һ������ְ�ɫ�������ǣ� ��
A. SO2 B. ��ͨNO2 ,��ͨSO2 C. ��ͨSO2����ͨH2S D. NH3,CO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�㶹���ǹ㷺������ֲ���е�һ����廯��������й����ԣ��еĻ����п������������á����ĺ��Ľṹ�Ƿ�������A�������ʽΪC9H6O2���÷�������A�����в���ת��Ϊˮ���ᡢ�Ҷ�������ʡ�
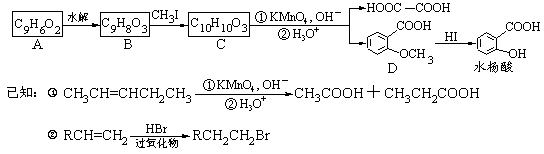
49��д��������A�Ľṹ��ʽ_____________________��
50������ת�������У�����ȡ����Ӧ����____������Ӧ����B��C��Ŀ����______________��
51��������D�ж���ͬ���칹�壬����һ��ͬ���칹���DZ��Ķ�ȡ�����ˮ������ɵIJ���֮һ�ܷ���������Ӧ������ͬ���칹��(����C��O��O���ṹ)����_____�֡�
52������A��B��C�������ʣ�������Լ���________��ѡ���ţ���
a������FeCl3��Һ������Cu(OH)2����Һ b������FeCl3��Һ������KMnO4��Һ
c������FeCl3��Һ��NaOH��Һ d������FeCl3��Һ������NaHCO3��Һ
53����ƺ����������� �ϳ�
�ϳ� ��д����ػ�ѧ��Ӧ���̣����Լ���ȡ����
��д����ػ�ѧ��Ӧ���̣����Լ���ȡ����
���úϳ�·������ͼ��ʾΪ��A B����
B���� Ŀ������
Ŀ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���ڳ�����0.1 mol��L��1��ˮ��0.1 mol��L��1���ᣬ����˵����ȷ����
A��0.1 mol��L��1��ˮ����Һ��pH=13
B��0.1 mol��L��1��ˮ��ˮϡ�ͣ���Һ��c(H+)��c(OH��)����С
C��0.1 mol��L��1������Һ�У�c(H+)��c(CH3COO��)
D��0.1 mol��L��1������0.1 mol��L��1NaOH��Һ��������������Һ�У�
c(Na+)��c(CH3COO��)��c(OH��)��c(H+)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
X��Y��Z��������Ԫ�أ���֪X����Y��������ͬ���Ӳ�ṹ��ZԪ��ԭ�Ӻ˵������YԪ��ԭ�Ӻ˵������9��Y����һ�������¿ɱ�������YZ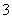 ��������˵����ȷ����
��������˵����ȷ����
A��X��Y��Z�����ڶ�����Ԫ�� B�����Ӱ뾶X��>Y��
C��Y����̬�⻯����γ����
D��X��Y��Z����Ԫ����ɵĻ������мȺ������Ӽ��ֺ��й��ۼ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���л�ѧ������ȷ����
A.��ϩ�Ľṹ��ʽ��CH2CH2
B.��Ȳ�ķ���ʽ��C2H2
C.˳-2-��ϩ�Ľṹ��ʽ��H3CHHCH3
D.�����ʵ��ʽ��C2H4O2
����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com