
| ||
| ||
| ||
| ||


科目:高中化学 来源: 题型:
 在一定条件下,将H2和N2置于一容积为2L的密闭容器中发生反应.反应过程中H2、N2和NH3的物质的量变化如图:
在一定条件下,将H2和N2置于一容积为2L的密闭容器中发生反应.反应过程中H2、N2和NH3的物质的量变化如图:查看答案和解析>>
科目:高中化学 来源: 题型:
| 化学式 | H2CO3 | CH3COOH | NH3?H2O |
| 电离常数 | K1=4.4×10-7 K2=4.7×10-11 |
K=1.75×10-5 | K=1.75×10-5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
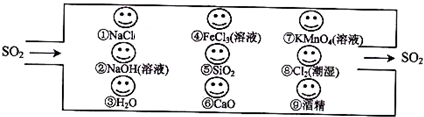
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、浓硫酸具有吸水性,因而能使蔗糖炭化 |
| B、浓硫酸具有吸水性可用作干燥剂,能够干燥氨气、氢气等气体 |
| C、Zn、Fe等金属与硝酸反应制取H2 |
| D、浓硝酸、浓硫酸在常温下能够使铁、铝等金属形成致密氧化膜而钝化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③ | B、②④ |
| C、①②③ | D、①②③④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com