
下列实验操作不正确的是( )
A.NaCl溶液蒸发结晶时,蒸发皿中有晶体析出并剩余少量液体时即停止加热
B.除去Fe(OH)3胶体中混有的Cl?离子,可用渗析的方法
C.蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处
D.用四氯化碳萃取碘时,碘的四氯化碳溶液从分液漏斗上口倒出
科目:高中化学 来源:2016届甘肃省嘉峪关市高一上学期期中考试化学试卷(解析版) 题型:选择题
下列各物质,按单质、化合物、混合物的顺序排列的是( )
A.干冰、铁、胆矾 B.液态氧、氧化钙、石灰水
C.氮气、氯化氢、烧碱 D.水、碘酒、熟石灰
查看答案和解析>>
科目:高中化学 来源:2016届湖北省高一上学期期末考试化学试卷(解析版) 题型:选择题
下列反应中,不能说明SO2是酸性氧化物的是
A.SO2+H2O H2SO3
H2SO3
B.SO2+2NaOH=Na2SO3+H2O
C.2SO2+O2 2SO3
2SO3
D.SO2+CaO=CaSO3
查看答案和解析>>
科目:高中化学 来源:2016届湖北省高一上学期期中考试化学试卷(解析版) 题型:填空题
铜器久置于空气中会和空气中的水蒸气、CO2、O2作用产生“绿锈”,该“绿锈”俗称“铜绿”,又称“孔雀石”[化学式为Cu2(OH)2CO3],“铜绿”能跟酸反应生成铜盐、CO2和H2O。某同学利用下述系列反应实现了“铜→铜绿→……→铜”的转化。
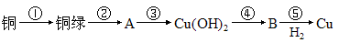
(1)从三种不同分类标准回答,“铜绿”属于哪类物质?___________________________。
(2)请写出②处的离子方程式。______________________________________________________________,
(3)上述转化过程中属于氧化还原反应的是_________(填序号,下同),属于复分解反应的是__________。
查看答案和解析>>
科目:高中化学 来源:2016届湖北省高一上学期期中考试化学试卷(解析版) 题型:选择题
过氧化氢(O为—1价)在二氧化锰催化作用下分解放出氧气的反应机理如下:
①MnO2 + H2O2 + 2H+ = Mn2+ + O2↑ + 2H2O ②Mn2+ + H2O2 = MnO2 + 2H+
下列说法正确的是( )
A.H2O2在①中是氧化剂,在②中是还原剂
B.在①中每生成1 mol O2,转移的电子数为1.204×1024
C.Mn2+在①中是还原产物,在②中是氧化产物
D.在二氧化锰催化作用下,1 mol H2O2分解生成22.4 L O2
查看答案和解析>>
科目:高中化学 来源:2016届湖北省高一上学期期中考试化学试卷(解析版) 题型:选择题
下图表示的一些物质或概念间的从属关系中正确的是
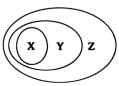
XYZ
A氧化钙氧化物碱性氧化物
B盐化合物电解质
C胶体分散系混合体系
D置换反应氧化还原反应离子反应
查看答案和解析>>
科目:高中化学 来源:2016届湖北省高一上学期期中考试化学试卷(解析版) 题型:填空题
(1)将ag氯化钙溶于1.8L水中,恰好使钙离子数与水分子数之比为1:100,则a值为 。
(2)在反应2A+B=3C+2D中,已知3.4gA与3.2gB完全反应,生成4.8gC,又知道D的式量为18,则B的式量是
(3)25.4g 某二价金属氯化物(ACl2)中含有0.4mol Cl-,则ACl2的摩尔质量是 ;A的相对原子质量是 ;ACl2的化学式是 。
(4) 某混合物由Na2SO4、Al2(SO4)3组成,已知Na、Al两元素的质量之比为23: 9,则Na2SO4和Al2(SO4)3物质的量之比为 ,含1.00mol SO42–的该混合物的质量为 。
查看答案和解析>>
科目:高中化学 来源:2016届湖北省高一上学期期中考试化学试卷(解析版) 题型:选择题
下列从混合物中分离出其中的一种成分,所采取的分离方法正确的是 ( )
A.由于碘在酒精中的溶解度大,所以可用酒精把碘水中的碘萃取出来
B.水的沸点为100oC,酒精的沸点为78.5oC,所以可用加热蒸馏方法,使含水的酒精变为无水酒精
C.四氯化碳和水混合后,可用分液的方法来分离
D.NaCl溶解度随温度下降而减小,所以用冷却法从热的含少量KNO3的NaCl溶液中分离得到纯净的NaCl
查看答案和解析>>
科目:高中化学 来源:2016届海南省琼海市高一上学期段考化学试卷(解析版) 题型:选择题
下列溶液中,Na+的物质的量浓度最大的是( )
A.1 mL 0.5 mol·L-1的NaNO3溶液 B.100 mL 0.01 mol·L-1的NaCl溶液
C.100 mL 0.1 mol·L-1的NaOH溶液 D.10 mL 0.1 mol·L-1的Na2SO4溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com