
 CO2(g) + H2(g) ��H �� 0�����д�ʩ����߷�Ӧ���ʵ��� ��������ѡ��
CO2(g) + H2(g) ��H �� 0�����д�ʩ����߷�Ӧ���ʵ��� ��������ѡ��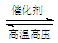 2NH3
2NH3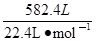 =26mol
=26mol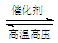 2NH3��ע��÷�ӦΪ���淴Ӧ����
2NH3��ע��÷�ӦΪ���淴Ӧ����


| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��(a)(b)��(c) | B��(a)��(c) | C��(b)��(d) | D��ȫ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���ԣ�D��=0.6mol/��L?min�� | B���ԣ�B��=0.45mol/��L?s�� |
| C���ԣ�C��=0.40mol/��L?min�� | D���ԣ�A��=0.2mol/��L?s�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ��ʴ���
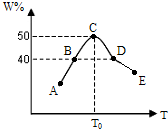
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
| ʱ��t/s | 0 | 50 | 150 | 250 | 350 |
| n��PCL3��/mol | 0 | 0.16 | 0.19 | 0.2 | 0.2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
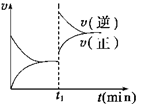
A��2A(g) + B(g) 2C(g) ��H>0 2C(g) ��H>0 |
B��2SO2(g)+ O2(g)  2SO3(g)��H<0 2SO3(g)��H<0 |
C��H2(g) + I2(g)  2HI(g)��H>0 2HI(g)��H>0 |
D��4NH3(g)+ 5O2(g)  4NO(g) + 6H2O(g)��H<0 4NO(g) + 6H2O(g)��H<0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 xC(g)��D(s)����t2��t3ʱ�̷ֱ�ı䷴Ӧ��һ������(�¶ȡ������������һ������)�����������C(g)��Ũ����ʱ��仯��ͼ��ʾ���й�˵����ȷ����
xC(g)��D(s)����t2��t3ʱ�̷ֱ�ı䷴Ӧ��һ������(�¶ȡ������������һ������)�����������C(g)��Ũ����ʱ��仯��ͼ��ʾ���й�˵����ȷ���� 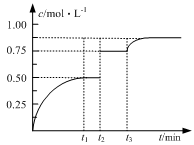
| A����Ӧ����ʽ��x��1 |
| B��t2ʱ�̸ı��������ʹ�ô��� |
| C��t3ʱ�̸ı����������ȥ����D |
| D��t1��t3��÷�Ӧ��ƽ�ⳣ������ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
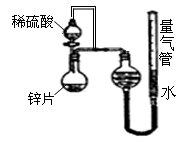
| ��� | ��(H2SO4)/mL | C(H2SO4)/mol��L-1 | t/s |
| �� | 10 | 1 | t1 |
| �� | 10 | 3 | t2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 N2��g��+2CO2��g��������˵������ȷ����
N2��g��+2CO2��g��������˵������ȷ����| A��ʹ���ʵ��Ĵ������ı䷴Ӧ���� | B������ѹǿ����߷�Ӧ���� |
| C�������¶�����߷�Ӧ���� | D���ı�ѹǿ�Է�Ӧ������Ӱ�� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com