
【题目】含同一元素的常见物质A、B、C,有如下转化关系(条件未标注):
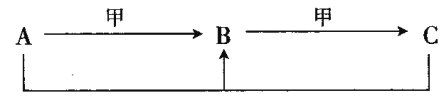
(1)当甲是KOH时,白色沉淀B为_____________。
(2)当甲为H2O时,气体B为______________。
(3)当A为Na时,单质甲为________________。
(4)当A为NH3时,气体单质B为_______________。
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】以下反应最符合绿色化学原子经济要求的是( )
A. 乙烯聚合为聚乙烯高分子材料
B. 甲烷与氯气制备一氯甲烷
C. 以铁和浓HNO3为原料生产硝酸铁
D. 用碳来还原氧化铁
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用辉铜矿(主要成分为Cu2S,含少量Fe2O3、SiO2等杂质)制备碱式碳酸铜的主要实验流程如下。

(1)滤渣Ⅰ的成分为MnO2、单质S和 (写化学式);硫酸浸取时,Cu2S被MnO2氧化的化学方程式为 。
(2)浸取时,Fe2O3溶于硫酸的离子方程式为 ;研究发现若先除铁再浸取,浸取速率明显变慢,其可能原因是 。
(3)“赶氨”时,最适宜的操作方法是 。
(4)滤液Ⅱ经蒸发结晶得到的盐主要是 (写化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯的产量可以用来衡量一个国家的石油化工发展水平。回答下列问题:
(1)乙烯的电子式为 ,结构简式为 。
(2)下列可以鉴别甲烷和乙烯的试剂为 (填选项字母)。
A.稀硫酸 B.溴的四氯化碳溶液 C.水 D.酸性高锰酸钾溶液
(3)下列物质中,不能通过乙烯加成反应得到的是 (填选项字母)。
A.CH3CH3 B.CH3CHCl2 C.CH3CH2OH D.CH3CH2Br
(4)已知2CH3CHO+O2![]() 2CH3COOH,以乙烯为主要原料合成乙酸,合成线路如下图所示:
2CH3COOH,以乙烯为主要原料合成乙酸,合成线路如下图所示:
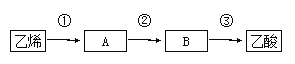
反应③的反应类型为 反应,反应②的化学方程式为 。
(5)工业上以乙烯为原料可以生产一种重要的合成有机高分子化合物,该反应类型为 反应,其反应的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知25℃、101kPa下,如图所示,石墨的燃烧热为393.5kJ/mol,金刚石的燃烧热为395.0kJ/mol.下列说法或表达正确的是( )
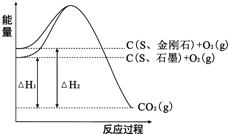
A.金刚石比石墨稳定
B.C(s、石墨)=C(s、金刚石) △H=+1.5kJ/mol
C.△H1<△H2
D.如果使用催化剂,△H1和△H2都变小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2O2是绿色氧化剂,且酸性介质下有更强的氧化性;易溶于水显弱酸性,常温下K1=1×10-12,K2=1×10-25。回答下列问题:
(1)常温下水的电离平衡常数K约为____________,K、K1、K2从大到小顺序为____________。
(2)在硫酸亚铁存在条件下,H2O2溶液可以把苯(C6H6)氧化为苯酚(C6H5OH)。反应后的混合物经过__________、蒸馏得到苯酚;理论上制取1mol苯酚需要消耗H2O2_______mol,实际消耗大于理论用量的主要原因是________________。
(3)K4[Fe(CN)6](黄色溶液)、K3[Fe(CN)6](黄绿色溶液)与一定量H2O2组成的混合物,用酸或碱调节混合溶液的pH,会出现黄色、黄绿色交替变化。按照从酸性至碱性的顺序,可观察到的现象是______________。
(4)工业用H2O2除去废水中的Cl2,氧化产物是__________;与SO2除Cl2相比,其优点是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语正确的是( )
A.聚丙烯的结构简式:![]()
B.丙烷分子的比例模型:![]()
C.四氯化碳分子的电子式:![]()
D.2﹣乙基﹣1,3﹣丁二烯分子的键线式:![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com