
【题目】我国新修订的《环境保护法》,使环境保护有了更严格的法律依据.
(1)往燃煤中加入 , 可大大减少烟气中的SO2含量.
(2)漂白粉用于生活用水的杀菌消毒,漂白粉的有效成分是(填化学式).
(3)废旧电池处理不当易造成重金属污染,治理废水中的重金属污染物可用沉淀法.例如,往含铅(Pb2+)废水中加入Na2S使Pb2+转变为(填化学式)沉淀而除去.
(4)北京和张家口市已成功申办2022年冬奥会,目前北京市政府正在全力改善空气质量,下列指标不在空气质量报告范围内的是(填字母).a.SO2浓度 b.CO2浓度 c.可吸入颗粒物
(5)硝酸型酸雨的形成主要是由汽车排放的尾气所致,汽车尾气中的氮氧化物可以用氨气来处理.例如,氨气与二氧化氮在催化剂作用下反应生成的均是对空气无污染的物质,请写出此时氨气与二氧化氮反应的化学方程式: .
【答案】
(1)石灰石(CaCO3)或生石灰(CaO)
(2)Ca(ClO)2
(3)PbS
(4)b
(5)6NO2+8NH3 ![]() 7N2+12H2O
7N2+12H2O
【解析】解:(1)煤燃烧过程中能生成二氧化硫,二氧化硫有毒,能污染环境,生石灰能够和生成的二氧化硫反应,从而防止二氧化硫污染空气,也可加入碳酸钙;所以答案是:石灰石(CaCO3)或生石灰(CaO);(2)漂白粉的有效成份是Ca(ClO)2 , 所以答案是:Ca(ClO)2;(3)往含铅(Pb2+)废水中加入Na2S可生成PbS沉淀,所以答案是:PbS;(4)二氧化碳无毒,不属于空气污染物,则没有列入我国空气质量报告,而二氧化硫、一氧化氮、二氧化氮都列入我国空气质量报告中,所以答案是:b;(5)氨气与二氧化氮反应生成氮气和水,方程式为6NO2+8NH3 ![]() 7N2+12H2O,所以答案是:6NO2+8NH3
7N2+12H2O,所以答案是:6NO2+8NH3 ![]() 7N2+12H2O.
7N2+12H2O.


科目:高中化学 来源: 题型:
【题目】合成氨及其相关工业中,部分物质间的转化关系如下:

下列说法正确的是
A. 反应I、Ⅱ、Ⅲ、V均属于氧化还原反应
B. 甲、乙、丙和丁四种物质中都含有氮元素
C. 反应Ⅳ和Ⅵ中的部分产物可在上述流程中循环利用
D. 反应V是先向饱和氯化钠溶液中通CO2至饱和再通NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(Ⅰ)气体制备时须先检查装置的气密性,下列各图所示装置,肯定不符合气密性检查要求的是 .
(Ⅱ)下面是中学化学实验中常见的几种仪器:
a.量筒 b.容量瓶 c.分液漏斗 d.托盘天平 e.温度计
(1)其中标示出仪器使用温度的是 (填编号).
(2)称取10.5g固体样品(1g以下使用游码)时,将样品放在了天平的右盘,则所称样品的实际质量为 g.
(3)使用前要检查仪器是否漏液的是 (填编号).
(Ⅲ)实验室需要95mL 1.0molL﹣1稀硫酸,现用98%的浓硫酸(其密度为1.84g/mL)来进行配制.若实验仪器有:
A.100mL量筒 B.托盘天平 C.玻璃棒 D.250mL容量瓶
E.10mL量筒 F.胶头滴管 G.50mL烧杯 H.100mL容量瓶
(1)需量取浓硫酸的体积为 mL.
(2)实验时选用的仪器有(填序号)
(3)配制过程中,下列情况会使配制结果偏高的是(填序号)
A.将稀释的硫酸液转移至容量瓶后,未洗涤烧杯和玻璃棒.
B.将烧杯内的稀硫酸向容量瓶中转移时,因操作不当使部分稀硫酸溅出瓶外.
C.未冷却至室温就定容.
D.用胶头滴管加水时,俯视观察溶液凹液面与容量瓶刻度相切.
E.容量瓶使用时未干燥
F.定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写正确的是( )
A.钠和水反应:2Na+2H2O═2Na++2OH﹣+H2↑
B.碳酸钙与稀醋酸的反应:CO ![]() +2H+═CO2↑+H2O
+2H+═CO2↑+H2O
C.铜与稀硝酸的反应:Cu+2H+═Cu2++H2↑
D.常温下,用氢氧化钠溶液吸收多余的氯气:Cl2+OH﹣═Cl﹣+ClO﹣+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将 H2S、 SO2、 SO3 各0.01mol依次溶解于1L水中,则该溶液具有
A. 中性、漂白性B. 酸性、漂白性C. 只有酸性D. 只有漂白性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物C是一种医药中间体,可通过下列方法合成:
(1)A中含氧官能团的名称为和 .
(2)B的结构简式为 .
(3)B→C的反应类型为 .
(4)C的同分异构体D能发生银镜反应,能与FeCl3溶液发生显色反应,且1molD最多能与2molNaOH反应.D分子中有4种不同化学环境的氢.请写出D的一种结构简式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用软锰矿(MnO2)、黄铁矿(FeS2)酸浸生产硫酸锰(MnSO4),并进一步电解制取电解二氧化锰(EMD)的工艺流程如下:
I. 将软锰矿、黄铁矿和硫酸按一定比例放入反应釜中,搅拌,加热保温反应一定时间。
II. 向反应釜中加入MnO2、CaCO3试剂,再加入Na2S溶液除掉浸出液中的重金属。
III. 过滤,向滤液中加入净化剂进一步净化,再过滤,得到精制MnSO4溶液。
IV. 将精制MnSO4溶液送入电解槽,电解制得EMD。
请回答下列问题:
(1)步骤I中搅拌、加热的目的是。完成酸浸过程中反应的离子方程式:
FeS2 + MnO2 + = Mn2+ + Fe2+ + S + SO42-+
(2)加入CaCO3将浸出液pH调至pH=5,从而除掉铁,请解释用CaCO3除铁的原理:。(结合离子方程式解释)
(3)步骤IV中用如图所示的电解装置电解精制的MnSO4溶液,生成EMD的是极(填“a”或“b”),生成EMD的电极反应式是。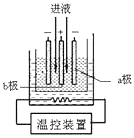
(4)EMD可用作碱性锌锰电池的材料。已知碱性锌锰电池的反应式为:Zn+2MnO2+2H2O=2MnOOH+Zn(OH)2。
下列关于碱性锌锰电池的说法正确的是_______(填字母序号)。
A.碱性锌锰电池是二次电池
B.碱性锌锰电池将化学能转化为电能
C.正极反应为:2MnO2+2H2O+2e-=2MnOOH+2OH-
D.碱性锌锰电池工作时,电子由MnO2经外电路流向Zn极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向某NaOH溶液中通入CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同。若向M中逐滴加入盐酸,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系有下列图示四种情况,且(2)、(3)、(4)图中分别有OA﹕AB=2﹕3, OA=AB, OA﹕AB=3﹕2,则下列分析与判断不正确的是(忽略CO2的溶解)( )

A. M中只有一种溶质的有(1)和(3)
B. M中有两种溶质的有(2)和(4)
C. (2)图显示M中的溶质为NaHCO3和Na2CO3,二者的物质的量之比为2:1
D. (4)图显示M中的溶质为NaOH和Na2CO3,二者的物质的量之比为1:2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com