
【题目】将4molA气体和2molB气体在2L的容器中混合,并在一定条件下发生反应2A(g)+B(g) ![]() 2C(g),若经2s后测得C的浓度为0.6mol·L-1,下列几种说法不正确的是( )
2C(g),若经2s后测得C的浓度为0.6mol·L-1,下列几种说法不正确的是( )
①用物质A表示的平均反应速率为0.3mol·L-1·s-1
②用物质B表示的平均反应速率为0.6mol·L-1·s-1
③2s时物质A的转化率为70% ④2s时物质B的浓度为0.7mol·L-1
A.①③ B.①④ C.②③ D.③④
【答案】C
【解析】
试题分析:将4mol A气体和2mol B气体在2L的密闭容器中混合并在一定条件下发生如下反应2A(g)+B(g)![]() 2C(g),若经2s(秒)后测得 C 的浓度为0.6molL-1s-1 ,依据化学平衡三段式列式计算。
2C(g),若经2s(秒)后测得 C 的浓度为0.6molL-1s-1 ,依据化学平衡三段式列式计算。
2A(g)+B(g)![]() 2C(g)
2C(g)
起始量(mol) 4 2 0
变化量(mol) 1.2 0.6 1.2
2s末(mol) 2.8 1.4 2L×0.6mol/L=1.2mol
①用物质A表示反应的平均速率=![]() =0.3mol/(Ls),故①正确;②用物质B表示反应的平均速率=
=0.3mol/(Ls),故①正确;②用物质B表示反应的平均速率=![]() =0.15mol/Ls,故②错误;③2s末物质A的转化率=
=0.15mol/Ls,故②错误;③2s末物质A的转化率=![]() ×100%=30%,故③错误;④2s末物质B的浓度=
×100%=30%,故③错误;④2s末物质B的浓度=![]() =0.7molL-1,故④正确;故选C。
=0.7molL-1,故④正确;故选C。


科目:高中化学 来源: 题型:
【题目】化学与社会、生产、生活密切相关。下列说法正确的是
A. 神舟10号飞船所用太阳能电池板的材料是单晶硅
B. 用于制作集成电路板的酚醛树脂是天然高分子化合物
C. 工业上获得大量乙烯、丙烯、丁二烯的方法是石油裂化
D. 日常生活中人们大量使用铝制品,是因为常温下铝不能与氧气反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取1.43 g Na2CO3·xH2O溶于水配成10 mL溶液,然后逐滴滴入稀盐酸直至没有气体放出为止,用去盐酸2.0 mL,并收集到112 mL CO2(标准状况)。试计算:
⑴ CO2的物质的量
⑵ Na2CO3·xH2O的物质的量。
⑶ x的值。
⑷所用稀盐酸的物质的浓度。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把7.2g铁粉投入40mL某HNO3溶液中,充分反应后剩余固体1.6g,产生NO2和NO的混合气体0.08mol。若不考虑N2O4的存在,则原HNO3溶液的物质的量浓度( )
A.3.5mol·L-1 B.4.5mol·L -1 C.7.0mol·L -1 D.9.0mol·L -1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨氧燃料电池具有很大的发展潜力,其工作原理如图所示。下列有关该电池的说法错误的是
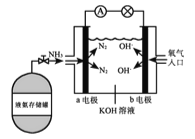
A.该电池工作时,溶液的pH不变
B.a电极为负极,b电极为正极
C.电子从a电极流出,经过导线到达b电极
D.电池总反应为4NH3+3O2=2N2+6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关叙述正确的是
A、地震发生后,灾区急需大量消毒剂,其中SO2可用于环境消毒
B、乙烯能使溴水和酸性高锰酸钾溶液褪色,其褪色原理相同
C、利用太阳能等清洁能源代替化石燃料,有利于节约能源,保护环境
D、工业上用二氧化硅在高温下与焦炭反应制得高纯度的硅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】很多鲜花和水果的香味都来自酯的混合物。下图是乙烯等为原料制取乙酸乙酯的过程(部分产物和反应条件已略去)。

请回答下列问题:
(1)B的结构简式为 。
(2)乙烯与水反应生成A的反应类型为 。
(3)A与C反应生成乙酸乙酯的化学方程式为 ,其反应类型为 。
(4)实验室可用右图装置制取乙酸乙酯。
①在试管a中加好相关试剂后,还需要加入2—3块的碎瓷片,其作用是 。
②试管b中盛有饱和碳酸钠溶液,生成的乙酸乙酯在该溶液的 (填“上”或“下”)层,用分液的方法分离出该产品所需的主要仪器是 。试管b中的导管口应在液面上方而不伸入到液面以下,其原因是 。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关组成生物体的化学元素和化合物的叙述,正确的是( )
A. 酶和核酸都是含有N元素的生物大分子
B. 组成核糖和核苷酸的化学元素完全相同
C. 肌肉细胞中含量最多的化合物是蛋白质
D. 人、动物与植物所含的化学元素的种类差异很大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA表示阿伏加德罗常数的值。下列说法中正确的是
①常温下,0.1molCl2与足量NaOH溶液反应,转移的电子数目为0.2NA
②常温常压下,18gH2O中含有的电子总数为10NA
③将100 mL 0.1 mol·L-1FeCl3溶液滴入沸水中可制得Fe(OH)3胶粒0.01NA
④在反应KIO3+6HI==KI+3I2+3H2O中,每生成3 mol I2转移的电子数为5NA
⑤常温常压下,14g的C2H4和C4H8混合气体中含有的原子数为3NA
⑥在标准状况下,0.5molNO与0.5molO2混合后气体分子数为0.75 NA
⑦1.0L 1.0 mol·L-1 Na2SiO3水溶液中含有的氧原子数为3NA
A.①⑤⑦ B.③④⑥
C.②④⑤ D.②③⑦
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com