
| A、该物质中铁元素的化合价为+2价 |
| B、该物质的化学式组成可表示为:Na20.3FeO.Fe2O3.8SiO2.H2O |
| C、1mol该物质能和18mol HNO3反应,也能与18mol HCl反应 |
| D、这种石棉属于新型无机非金属材料 |


 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:高中化学 来源: 题型:
| A、红色激光束能透过小烧杯中的氢氧化铁胶体,但不能透过小烧杯中较浓的硫酸铜溶液 |
| B、胶体的丁达尔效应是胶体粒子对可见光散射而形成的 |
| C、胶体化学是随20世纪未纳米科技兴起而产生的 |
| D、纳米粒子的大小与胶体粒子相当,但纳米粒子的体系不一定是胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
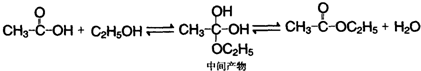
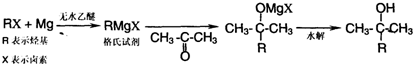
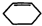 )为原料,通过以下各步转化,最终可制得有机物
)为原料,通过以下各步转化,最终可制得有机物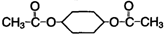 (部分反应过程及反应条件略去)
(部分反应过程及反应条件略去)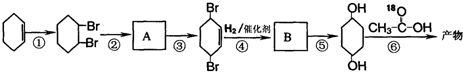
查看答案和解析>>
科目:高中化学 来源: 题型:
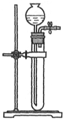 检查装置气密性是化学实验中的重要操作之一.按要求回答下列问题:
检查装置气密性是化学实验中的重要操作之一.按要求回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
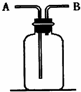 根据正放在桌面上的如图装置,回答下列问题:
根据正放在桌面上的如图装置,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
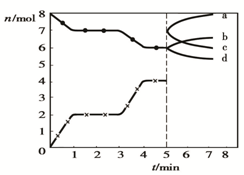 炼铁的还原剂CO是由焦炭和CO2反应而得,现将焦炭和CO2放入体积为2L的密闭容器中,高温下进行下列反应:C(s)+CO2(g)?2CO(g)△H=Q kJ/mol.如图为CO2、CO的物质的量n随时间t的变化关系图,下列说法正确的是( )
炼铁的还原剂CO是由焦炭和CO2反应而得,现将焦炭和CO2放入体积为2L的密闭容器中,高温下进行下列反应:C(s)+CO2(g)?2CO(g)△H=Q kJ/mol.如图为CO2、CO的物质的量n随时间t的变化关系图,下列说法正确的是( )| A、0~1min,v(CO)=1mol/(L?min);1~3min时,v(CO)=v(CO2) | ||||
B、当容器内的压强不变时,反应一定达到平衡状态,且
| ||||
C、3min时温度由T1升高到T2,则Q>0,重新平衡时
| ||||
| D、5min时再充入一定量的CO,a、b分别曲线表示n(CO)、n(CO2)的变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
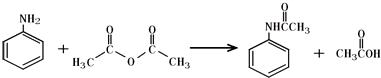
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Cu2+、Na+、SO42-、Cl- |
| B、K+、H+、HCO3-、NO3- |
| C、OH-、HCO3-、Ca2+、Na+ |
| D、Ba2+、Na+、OH-、NO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com