
某溶液的溶质是由下列中的几种离子构成:Na+、Fe3+、Cu2+、Ba2+、CO32-、AlO2-、SO32-、SO42-。取该溶液进行有关实验,实验步骤及结果如下:
①向溶液中加入过量稀盐酸,得到气体甲和溶液甲;
②向溶液甲中加入过量NH4HCO3溶液,得到白色沉淀乙、气体乙和溶液乙;
③向溶液乙中加入过量Ba(OH)2溶液,得到白色沉淀丙、气体丙和溶液丙。
④检验气体甲、气体乙、气体丙,都只含有一种成份,而且各不相同。
请回答下列问题:
(1)只根据实验①能得出的结论是 ;
(2)沉淀丙中一定含有 ,可能含有 。
(3)该溶液中肯定存在的离子有 。
(4)气体甲的化学式为 ;气体乙的名称为 ;气体丙的分子几何构型是 ;
(5)向溶液甲中加入NH4HCO3溶液至过量,该过程中发生的离子方程式为 ; 。
(1)该溶液中至少还有CO32-、SO32-中的一种;一定不含Fe3+、Cu2+、Ba2+;
一定含有Na+.( 3分)
(2)BaCO3; BaSO4 (各1分)
(3)Na+、SO32-、AlO2- (2分)
(4)SO2 二氧化碳 三角锥形 (各1分)
(5)H++HCO3- CO2↑+H2O;(2分) Al3++3HCO3-
CO2↑+H2O;(2分) Al3++3HCO3- Al(OH)3↓+3CO2↑ (2分)
Al(OH)3↓+3CO2↑ (2分)
【解析】
试题分析:(1)由①向溶液中加入过量稀盐酸,得到气体甲和溶液甲,与盐酸反应产生气体的离子是CO32-、SO32-,所以只根据实验①能得出的结论是该溶液中至少还有CO32-、SO32-中的一种,含有二者中的一种,则与二者发生离子反应的离子不能存在,如Fe3+、Cu2+、Ba2+,所以该溶液中一定不存在Fe3+、Cu2+、Ba2+;则溶液中的阳离子只能是Na+;
(2)②向溶液甲中加入过量NH4HCO3溶液,得到白色沉淀乙、气体乙和溶液乙,说明该溶液中一定存在AlO2-,一定不存在碳酸根离子,所以一定存在亚硫酸根离子;③向溶液乙中加入过量Ba(OH)2溶液,得到白色沉淀丙、气体丙和溶液丙,因为上步中的试剂碳酸氢铵是过量的,则碳酸氢铵与氢氧化钡反应,一定有碳酸钡沉淀生成,所以沉淀丙中一定含有BaCO3;因为硫酸根离子不能确定,所以丙中可能含有BaSO4;
(3)根据以上分析,该溶液中肯定存在的离子有Na+、SO32-、AlO2-;
(4)④检验气体甲、气体乙、气体丙,都只含有一种成份,而且各不相同,所以甲气体是SO2,乙气体是二氧化碳,丙气体的氨气,氨气的空间构型是三角锥形;
(5)溶液甲中含有过量的盐酸及铝离子,所以加入NH4HCO3溶液至过量,发生的反应有盐酸与碳酸氢根离子的反应,离子方程式为H++HCO3- CO2↑+H2O;同时碳酸氢根离子与铝离子发生水解反应,离子方程式为Al3++3HCO3-
CO2↑+H2O;同时碳酸氢根离子与铝离子发生水解反应,离子方程式为Al3++3HCO3- Al(OH)3↓+3CO2↑。
Al(OH)3↓+3CO2↑。
考点:考查常见离子的性质,离子方程式的书写


科目:高中化学 来源:2015届辽宁省高一上学期期中考试化学试卷(解析版) 题型:选择题
下列离子方程式改写成化学方程式正确的是
A.Cu2+ +2OH- =Cu(OH)2 CuCO3+2NaOH=Cu(OH)2+Na2CO3
B.CO32- + 2H+ = CO2 + H2O BaCO3 + 2HCl =BaCl2+ CO2 + H2O
C.Ca2+ + CO32- = CaCO3 Ca(NO3)2+NaCO3 = CaCO3+NaNO3
D.H+ +OH- = H2O 2KOH+H2SO4 = K2SO4 +2H2O
查看答案和解析>>
科目:高中化学 来源:2015届辽宁省高三上学期10月月考试卷(解析版) 题型:选择题
下列有关物质分类或归类正确的一组是( )
①液氨、液氯、干冰、碘化银均为化合物 ②汽油、盐酸、水玻璃、氨水均为混合物
③明矾、小苏打、醋酸、次氯酸均为电解质 ④碘酒、牛奶、豆浆、漂粉精均为胶体
⑤Na2O2、Na2CO3、NaHCO3、Na2SiO3均为钠盐
A.①和② B.②和③ C.③和④ D.②③⑤
查看答案和解析>>
科目:高中化学 来源:2015届辽宁省分校高三上学期期初考试化学试卷(解析版) 题型:选择题
下列所指物质不属于纯净物的是( )
A.分子式为C2H4Cl2的物质
B.只含铁和氧两种元素且Fe的质量分数为72.41%的物质
C.干冰
D.按体积比为1:1混合NH3和HCl(同条件)
查看答案和解析>>
科目:高中化学 来源:2015届辽宁省分校高三上学期期初考试化学试卷(解析版) 题型:选择题
实验室制Cl2的反应为4HCl(浓)+MnO2 高温 MnCl2+C12↑+2H2O.下列说法错误的是( )
A.还原剂是HCl,氧化剂是MnO2
B.每生成1 molCl2,转移电子的物质的量为2 mol
C.每消耗1 molMnO2,起还原剂作用的HCl消耗4mol
D.生成的Cl2中,除含有一些水蒸气外,还含有HCl杂质
查看答案和解析>>
科目:高中化学 来源:2015届辽宁省大连市高三10月月考理综化学试卷(解析版) 题型:选择题
1 L某混合溶液中,溶质X、Y浓度都为0.1mol·L—1,向混合溶液中滴加0.1 mol·L—1某溶液Z,所得沉淀的物质的量如图所示,则X、Y、Z分别是
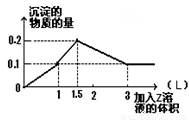
A.氯化铝、氯化镁、氢氧化钠 B.偏铝酸钠、氢氧化钡、硫酸
C.氯化铝、氯化铁、氢氧化钠 D.偏铝酸钠、氯化钡、硫酸
查看答案和解析>>
科目:高中化学 来源:2015届辽宁沈阳市高三上学期第一次模拟考试化学试卷(解析版) 题型:实验题
某研究小组为了探究一种无机矿物质X(仅含四种元素)的组成和性质,设计并完成如下实验:
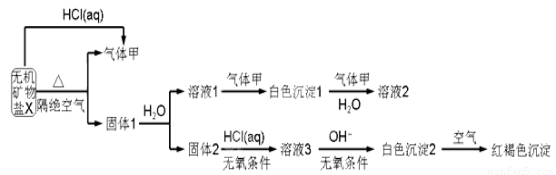
另取10.80gX在惰性气流中加热至完全分解,得到6.40g固体1.请回答如下问题:
(1)画出白色沉淀1中金属元素的原子结构示意图_______,写出气体甲的电子式_______。
(2)X的化学式是______,在惰性气流中加热X至完全分解的化学反应方程式为_______。
(3)白色沉淀2在空气中变成红褐色沉淀的原因是_______(用化学反应方程式表示)。
(4)一定条件下,气体甲与固体1中的某种成分可能发生氧化还原反应,写出一个可能的化学反应方程式_______,并设计实验方案验证该反应的产物_______。
查看答案和解析>>
科目:高中化学 来源:2015届辽宁沈阳市高三上学期第一次模拟考试化学试卷(解析版) 题型:选择题
水溶液中能大量共存的一组离子是
A.Na+、Ca2+、Cl-、SO42- B.Fe2+、H+ 、SO32-、ClO-
C.Mg2+、NH4+、Cl- 、SO42- D.K+、Fe3+、NO3-、SCN-
查看答案和解析>>
科目:高中化学 来源:2015届福建省高二上学期第二次月考化学试卷(解析版) 题型:选择题
可逆反应aA(g)+bB(g) cC(g)+dD(g) ΔH,同时符合下列两图中各曲线的是( )
cC(g)+dD(g) ΔH,同时符合下列两图中各曲线的是( )
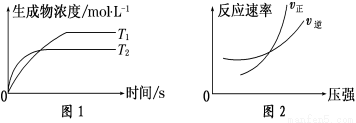
A.a+b>c+d T1>T2 ΔH>0 B.a+b>c+d T1<T2 ΔH<0
C.a+b<c+d T1>T2 ΔH>0 D.a+b<c+d T1<T2 ΔH<0
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com