
| A. | CuO | B. | Cu20 | C. | Cu | D. | Cu(OH)2CO3 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 胶体一定是均一、透明、介稳的 | B. | 用丁达尔效应区别胶体和溶液 | ||
| C. | 可以用滤纸来分离胶体和溶液 | D. | 胶体只能在液体中形成 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 .
.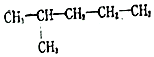 2-甲基戊烷
2-甲基戊烷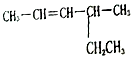 4-甲基-2-己烯.
4-甲基-2-己烯.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 水解达到平衡时(不饱和),加氯化铁溶液达饱和,溶液的酸性会增强 | |
| B. | 浓度为5 mol•L-1和0.5 mol•L-1的两种 FeCl3溶液,其他条件相同时,Fe3+的水解程度前者比后者小 | |
| C. | 有50℃和20℃的同浓度的两种FeCl3稀溶液,其他条件相同时,Fe3+的水解程度前者比后者小 | |
| D. | 为抑制 Fe3+的水解,较好地保存 FeCl3溶液,应加少量盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
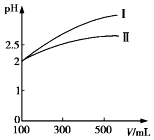 乙酸、氰酸、碳酸等都是重要的碳的化合物.己知如下信息:
乙酸、氰酸、碳酸等都是重要的碳的化合物.己知如下信息:| 弱酸的化学式 | CH3COOH | HCN | H2CO3 |
| 电离常数 | Ka=l.8×l0-5 | Ka=4.9×10-10 | Kal=4.3×10-7 Ka2=5.6×10-11 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
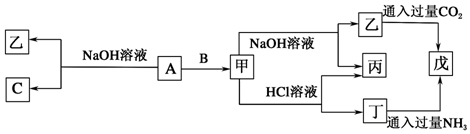
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com