
【题目】甲烷是一种高效清洁的新能源,0.25mol甲烷完全燃烧生成液态水时放出222.5KJ热量,则下列热化学方程式中正确的是( )
A.2CH4(g)+4O2(g)═2CO2(g)+4H2O(l);△H═+890KJ/mol
B.CH4(g)+2O2(g)═CO2(g)+2H2O(l);△H═+890KJ/mol
C.CH4(g)+2O2(g)═CO2(g)+2H2O(l);△H═﹣890KJ/mol
D.2CH4(g)+4O2(g)═2CO2(g)+4H2O(l);△H═﹣890KJ/mol
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案科目:高中化学 来源: 题型:
【题目】A与D是常见的有机化工原料,下列路线合成香料M(![]() ):
):

已知以下信息:
①A的相对分子质量为28
②2RCH2CHO![]()

(1)A的结构简式是________,D的名称是__________。
(2)A生成B的反应类型为_____________,G中官能团名称为___________。
(3)E生成F的的化学方程式为_________________________________________。
(4)下列关于G的说法正确的是______________。(填标号)
a.属于芳香烃
b.可与FeCl3溶液反应显紫色
c.1molG与H2完全加成,最多4molH2
d.可与新制的氢氧化铜共热生成红色沉淀
(5)化合物M的同系物N比M的相对分子质量大14,N的同分异构体中同时满足下列条件的共有__________种(不考虑立体构)。
①与化合物M含有相同的官能团; ②苯环上有两个邻位取代基
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在10 L恒容密闭容器中充入X(g)和Y(g),发生反应X(g)+Y(g) ![]() M(g)+N(g),所得实验数据如下表:
M(g)+N(g),所得实验数据如下表:
实验 编号 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量/mol | ||
n(X) | n(Y) | n(M) | |||
① | 700 | 0.40 | 0.10 | 0.090 | |
② | 800 | 0.10 | 0.40 | 0.080 | |
③ | 800 | 0.20 | 0.30 | a | |
④ | 900 | 0.10 | 0.15 | b | |
下列说法正确的是( )
A. 实验①中,若5 min时测得n(M)=0.050 mol,则0至5 min时间内,用N表示的平均反应速率v(N)=1.0×10-2 mol·L-1·min-1
B. 实验②中,该反应的平衡常数K=2.0
C. 实验③中,达到平衡时,X的转化率为60%
D. 实验④中,达到平衡时,b>0.060
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是
A. 氯气溶于水:Cl2 + H2O ![]() 2 H
2 H![]() + Cl
+ Cl![]() + ClO
+ ClO![]()
B. NH4HSO4溶液呈酸性的主要原因是:NH4++ H2O ![]() NH3·H2O+ H+
NH3·H2O+ H+
C. 酸性溶液中KIO3与KI反应生成I2:IO![]() + I
+ I![]() + 6 H
+ 6 H![]() = I2 + 3 H2O
= I2 + 3 H2O
D. NaHCO3溶液中加足量Ba(OH)2溶液:HCO![]() + Ba
+ Ba![]() + OH
+ OH![]() = BaCO3↓+ H2O
= BaCO3↓+ H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙两电池电极材料都是铁棒与碳棒,请回答下列问题:

(1)若两电池中均为CuSO4溶液,反应一段时间后:
①有红色物质析出的是甲池中的________棒,乙池中的________棒.(填“Fe”或“C”)
②乙池中的阳极反应式为:________________.
③乙池中总反应的化学方程式为:________________.
(2)若两池中均为饱和NaCl溶液,溶液中滴两滴酚酞.
①乙池中总的离子方程式为:________________.
②甲池C极上的电极反应式为:________________.
③甲池中首先出现红色的是_____极;乙池中首先出现红色的是______极(填“Fe”或“C”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤燃烧排放的烟气含有SO2和NOx,形成酸雨、污染大气,采用NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝,回答下列问题:
(1)NaClO2中氯元素的化合价为______________。
(2)在鼓泡反应器中通入含有SO2和NOx的烟气,反应温度为323 K,NaClO2溶液浓度为5×103mol/L,溶液呈碱性。反应一段时间后溶液中离子浓度的分析结果如下表
离子 | SO42 | SO32 | NO3 | NO2 | Cl |
c/(mol/L) | 8.35×104 | 6.87×106 | 1.5×104 | 1.2×105 | 3.4×103 |
①以NO转化为NO3-为例,写出NaClO2溶液脱硝过程中主要反应的离子方程式__________。增加压强,NO的转化率__________(填“提高”“不变”或“降低”)。
②随着吸收反应的进行,吸收剂溶液的pH逐渐___________(填“提高”“不变”或“降低”)。
③由实验结果可知,脱硫反应速率脱硝反应速率__________(填“大于”或“小于”)。原因是除了SO2和NO在烟气中的初始浓度不同,还可能是________________________________。
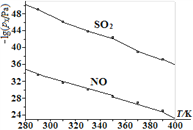
(3)在不同温度下,NaClO2溶液脱硫、脱硝的反应中,SO2和NO的平衡分压px如图所示。已知图中: ![]() 其中(nx代表各成分的物质的量,na代表气体总物质的量)
其中(nx代表各成分的物质的量,na代表气体总物质的量)
①由图分析可知,反应温度升高,脱硫、脱硝反应的平衡常数均____(填“增大”“不变”或“减小”)。
②反应ClO2+2SO32==2SO42+Cl的平衡常数K表达式为______________。
(4)如果采用NaClO、Ca(ClO)2替代NaClO2,也能得到较好的烟气脱硫效果。从化学平衡原理分析,Ca(ClO)2相比NaClO具有的优点是______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
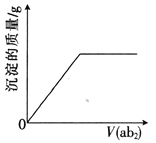
【题目】短周期主族元素a、b、c、d、e的原子序数依次增大,b是地壳中含量最高的元素,e的单质的熔点在同周期元素中最高,a、b的原子序数之和等于e的原子序数,d原子的核外电子层数等于最外层电子数:分别向cdb2溶液、c2eb3溶液中通入气体ab2,产生沉淀的质量与通入气体的体积的定性关系都可用右图表示。下列说法不正确的是
A. 原子半径:c>d>e>a>b
B. 工业上通常采用ab高温还原d2b3的方法冶炼d的单质
C. 同温下,0.1mol·L-1c2eb3溶液的pH大于0.1mol·L-1c2ab3溶液
D. 简单氢化物的热稳定性:b>a>e
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是部分短周期元素原子半径与原子序数的关系图.则下列说法正确的是( )

A. 简单离子的半径:X<Z<M
B. 最高价氧化物对应水化物的酸性:R<N
C. Y、R两种元素的气态氢化物稳定性:Y>R
D. 由X与N两种元素组成的化合物不能与任何酸反应,但能与强碱反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应原理中,不符合工业冶炼金属实际情况的是
A.2HgO![]() 2Hg+O2↑ B.4Al+3MnO2
2Hg+O2↑ B.4Al+3MnO2![]() 2Al2O3+3Mn
2Al2O3+3Mn
C.2MgO![]() 2Mg+O2↑ D.4CO+Fe3O4
2Mg+O2↑ D.4CO+Fe3O4![]() 3Fe+4CO2
3Fe+4CO2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com