
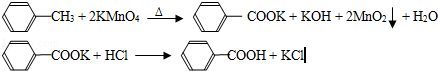
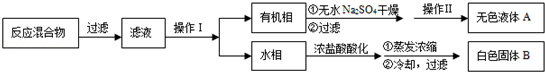
| ��� | ʵ�鷽�� | ʵ������ | ���� |
| �� | ����ɫ����B����ˮ�У������ܽ⣬��_________�� ��_________�� | �õ���ɫ�������ɫ��Һ | |
| �� | ȡ������Һ���Թ��У���_________�� | ���ɰ�ɫ���� | ��Һ��Cl�� |
| �� | �����ɫ���壬��_________�� | ��_________�� | ��ɫ�����DZ����� |
| ��� | ʵ�鷽�� | ʵ������ | ���� |
| �� | ����ɫ����B����ˮ�У����ȣ��ܽ⣬��ȴ������ | �õ���ɫ�������ɫ��Һ | |
| �� | ȡ������Һ���Թ��У����������������ữ��AgNO3��Һ | ���ɰ�ɫ���� | ��Һ����Cl�� |
| �� | �����ɫ���壬����ʹ���ڻ��������۵㣻 | �۵�Ϊ122.4�� | ��ɫ�����DZ����� |
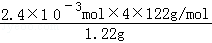 ��100%�� 96%
��100%�� 96%| ��� | ʵ�鷽�� | ʵ������ | ���� |
| �� | ����ɫ����B����ˮ�У����ȣ��ܽ⣬��ȴ������ | �õ���ɫ�������ɫ��Һ | |
| �� | ȡ������Һ���Թ��У����������������ữ��AgNO3��Һ | ���ɰ�ɫ���� | ��Һ����Cl�� |
| �� | �����ɫ���壬����ʹ���ڻ��������۵㣻 | �۵�Ϊ122.4�� | ��ɫ�����DZ����� |
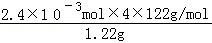 ��100%=96%��
��100%=96%��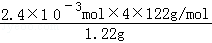 ��100%�� 96%
��100%�� 96%


| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 ��CH3CH2OH��CH3CH2Br��NH4Cl��Һ������ɫҺ�壬ֻ��һ���Լ����ܰ� ���Ǽ��������Լ���(����)
��CH3CH2OH��CH3CH2Br��NH4Cl��Һ������ɫҺ�壬ֻ��һ���Լ����ܰ� ���Ǽ��������Լ���(����)| A����ˮ���������������� | B��NaOH��Һ |
| C��Na2SO4��Һ | D��Br2��CCl4��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�ʵ����
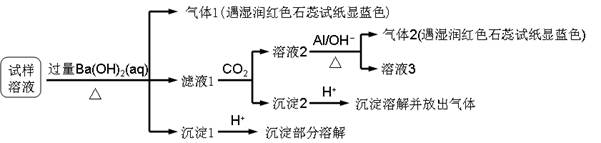
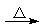 3NH3 + 8AlO2��
3NH3 + 8AlO2���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�ʵ����
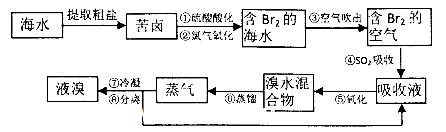
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����߸�����ص�������������Ũ�����ữ |
| B������Fe2����ˮ�⣬��ϡ�����ữ |
| C������ij±�������Ƿ���Ԫ�أ��ȼ�HNO3�ữ���ټ�AgNO3��Һ���� |
| D��ȷ����Һ�к���SO42��ʱ�����������ữ���ټ�BaCl2��Һ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������

| ���� | Mn(OH)2 | Co(OH)2 | Ni(OH)2 | MnS | CoS | NiS |
| Ksp | 2.1��10��13 | 3.0��10��16 | 5.0��10��16 | 1.0��10��11 | 5.0��10��22 | 1.0��10��22 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| | �١��� | �֡��� | �ᡡ�� |
| A | �ⶨ��Ũ�ȵ�Na2CO3��Na2SO3 ��Һ��pH | ǰ��pH�Ⱥ��ߵĴ� | �ǽ����ԣ� |
| B | ��ɫ��Һ�еμ���ˮ��CCl4�������� | �²���Һ����ɫ | ԭ��Һ���� |
| C | ����ҺX�м���ϡ���ᣬ������������ɫ����ͨ�����ʯ��ˮ�� | ���ɰ�ɫ���� | ��ҺX��һ������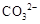 �� ��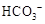 |
| D | ��ij��ɫ��Һ�еμ������ữ��BaCl2��Һ | ������ɫ���� | ��Һ�в�һ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| ѡ�� | ʵ����� | ���� | ���� |
| A | ���ܱ������м���CuO | ��ɫ�����ɺ�ɫ���� | CuO���ȷֽ�õ�����Cu |
| B | ��SO2ͨ��Ʒ����Һ�� | ��Һ��ɫ | SO2����Ư���� |
| C | ��Mg��Al��NaOH��Һ���ԭ��� | Al�缫�ܽ� | Al��Mg�������ǿ |
| D | ��ij��Һ�м��������ữ���Ȼ�����Һ | �а�ɫ�������� | ����Һ��һ������SO42- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
A�������������������Ƿ���ʣ�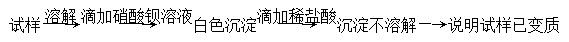 |
B����ȥ�����к��е����������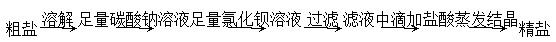 |
C������ij��Һ���Ƿ���Fe2�� |
| D��֤����������H2O2�������Ա�I2ǿ�� |
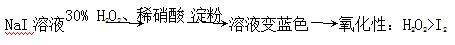
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com