
【题目】足量金属镁与一定量浓硝酸反应,得到硝酸镁溶液和NO2、NO的混合气体,这些气体与2.52LO2(标准状况)混合后通入水中.所有气体完全被水吸收生成硝酸.若向所得硝酸镁溶液中加入2.5mol/LNaOH溶液至Mg2+恰好完全沉淀,则消耗NaOH溶液的体积是( )
A.45mL
B.180mL
C.90Ml
D.135mL
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】A、B、C的结构简式如下:
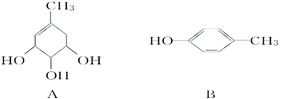
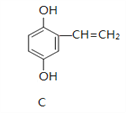
(1)A分子中含有的官能团的名称是_____________________;
(2)能与NaOH溶液反应的是_________(填“A”、“B”或“C”),写出与NaOH溶液反应的化学方程式_________________________________________。(任写一个)
(3)A在浓硫酸作用下加热可得到B,其反应类型是_________________。
(4)1 molC分别与浓溴水和H2反应时,最多消耗Br2 _____ mol、消耗H2 ____ mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】危化仓库中往往存有钠、钾、硫、白磷(P4)、硝酸铵和氰化钾(KCN)等危险品。请回答下列问题:
(1)NH4NO3为爆炸物,在某温度下按下式进行分解:5NH4NO3=4N2↑+2HNO3+9H2O则被氧化和被还原的氮元素质量之比为________;
(2)硫酸铜溶液是白磷引起中毒的一种解毒剂:1lP4+60CuSO4+96H2O=20Cu3P+24H3PO4+60H2SO4。若8molH3PO4生成,则被CuSO4氧化的P4的物质的量为______________mol;
(3)处理CN一常用的一种方法是用氯气氧化。若某厂废水中含KCN,其浓度为650mg / L。现用氯氧化法处理,发生如下反应(其中N均为-3价):KCN+2KOH+Cl2 = KOCN+2KCl+H2O 。若投入过量液氯,可将氰酸盐进一步氧化为无毒的N2和CO2。请写出该反应的化学方程式,____,若处理上述废水20 L,使KCN完全转化为无毒物质,至少需液氯_________ g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应2H2S+O2=2S↓+2H2O,4NaI+O2+2H2O=4NaOH+2I2和Na2S+I2=2NaI+S↓,下列氧化性大小关系正确的是
A. O2>I2>S B. I2>O2>S C. O2>S>I2 D. S>I2>O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科研人员研制出一种室温“可呼吸“Na—CO2"电池。放电时该电池“吸入” CO2,充电时“呼出” CO2。吸入CO2时,其工作原理如右图所示。吸收的全部CO2中,有 2/3转化为Na2CO3固体沉积在多壁碳纳米管(MWCNT)电极表面。下列说法正确的是

A. “吸入” CO2时的正极反应:4Na++ 3 CO2+ 4e -= 2Na2CO3+ C
B. “呼出” CO2时,Na+向多壁碳纳米管电极移动
C. “吸入” CO2时,钠箔为正极
D. 标准状况下,每“呼出”22.4 L CO2,转移电子数为0.75 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】测定CuSO4·xH2O晶体的x值,数据如表中所示,己知x的理论值为5.0,产生误差的可能原因是
坩埚质量 | 坩埚+试样 | 失水后,坩埚+试样 |
11.70g | 20.82g | 16.50g |
A. 晶体中含不挥发杂质 B. 未做恒重操作
C. 加热时有晶体溅出 D. 加热前晶体未研磨
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】几种短周期元素的原子半径及化合价见表:
元素代号 | A | B | D | E | G | H | I | J |
化合价 | ﹣1 | ﹣2 | +4、﹣4 | +6、﹣2 | +5、﹣3 | +3 | +2 | +1 |
原子半径/nm | 0.071 | 0.074 | 0.130 | 0.102 | 0.110 | 0.143 | 0.160 | 0.186 |
分析上表中有关数据,结合已学过的知识,回答以下问题.涉及上述元素的答案,请用元素符号表示.
(1)E元素在周期表中的位置是 .
(2)A,H,J对应的离子半径由大到小的顺序是(填写离子符号) .
(3)用电子式表示A与I所形成化合物的形成过程 .
(4)B与H所形成的化合物与J的最高价氧化物的水化物X的溶液发生反应的离子方程式为;
(5)用B与D所形成的化合物制备D单质的化学方程式为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com