
| A. | 相同温度下两种溶液的pH:Na2CO3>NaHCO3 | |
| B. | 若分别升高温度,两种溶液的pH均减小 | |
| C. | 若分别加入少量NaOH,两溶液中c(CO32-)均增大 | |
| D. | 两溶液中的离子浓度均存在关系:c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-) |
分析 A.碳酸根离子的水解程度大于碳酸氢根离子,则相同温度下两种溶液的pH:Na2CO3<NaHCO3;
B.升高温度促进水解,两溶液的pH应该增大;
C.NaOH抑制碳酸钠的水解,NaHCO3溶液中加入NaOH发生反应:OH-+HCO3-═CO32-+H2O,两溶液中c(CO32-)都增大;
D.根据碳酸钠、碳酸氢钠溶液中的电荷守恒判断.
解答 解:A.碳酸根离子的水解程度大于碳酸氢根离子,则Na2CO3溶液pH较大,故A正确;
B.盐类的水解为吸热反应,升高温度促进水解,溶液的pH增大,故B错误;
C.Na2CO3加入NaOH抑制水解,NaHCO3溶液中加入NaOH发生OH-+HCO3-═CO32-+H2O,两溶液中c(CO32-)均增大,故C正确;
D.两溶液都存在电荷守恒:c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-),故D正确;
故选B.
点评 本题考查离子浓度大小比较,为高频考点,题目难度中等,侧重于学生的分析能力的考查,注意掌握电荷守恒、盐的水解原理在判断离子浓度大小中的应用方法.


科目:高中化学 来源: 题型:选择题
| A. | 2H2(g)+O2(g)=2H2O(g)△H=-286 kJ/mol | B. | 2H2(g)+O2(g)=2H2O(g)△H=-572 kJ/mol | ||
| C. | H2(g)+$\frac{1}{2}$O2(g)=H2O(g)△H=-330 kJ/mol | D. | H2O(g)=H2(g)+$\frac{1}{2}$O2(g)△H=+242 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加热NH4C1晶体时,将湿润的红色石蕊试纸靠近试管口,检验NH3的生成 | |
| B. | 取少量溶液X,向其中加入适量新制氯水,再加几滴KSCN溶液,溶液变红,说明X溶液中一定含有Fe2+ | |
| C. | 除去KNO3中的少量NaCl,可将混合物制成热的饱和溶液,冷却结晶,过滤 | |
| D. | 通过灼热的镁粉除去N2中的O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 绿色化学的核心是利用化学原理从源头上减少和消除化学工业生产对环境的污染 | |
| B. | 对废旧电池进行回收处理主要是为了防止重金属污染水源和土壤 | |
| C. | 采用催化转换技术将汽车尾气中的NOx和CO转化为无毒气体 | |
| D. | PM2.5是指大气中直径接近于2.5×10-6m的细颗粒物,它们分散在空气中形成的混合物具有丁达尔效应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
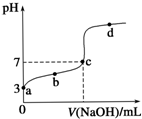 已知常温时CH3COOH的电离平衡常数为K.该温度下向20mL 0.1mol•L-1 CH3COOH溶液中逐滴加入0.1mol•L-1 NaOH溶液,其pH变化曲线如图所示(忽略温度变化).下列说法中错误的是( )
已知常温时CH3COOH的电离平衡常数为K.该温度下向20mL 0.1mol•L-1 CH3COOH溶液中逐滴加入0.1mol•L-1 NaOH溶液,其pH变化曲线如图所示(忽略温度变化).下列说法中错误的是( )| A. | a点表示的溶液中c(CH3COO-)略小于10-3 mol•L-1 | |
| B. | b点表示的溶液中c(CH3COO-)>c(Na+) | |
| C. | c点表示CH3COOH和NaOH恰好完全中和 | |
| D. | b、d点表示的溶液中$\frac{c(C{H}_{3}CO{O}^{-})•c({H}^{+})}{c(C{H}_{3}COOH)}$ 均等于K |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 ,AB2中的化学键是共价键
,AB2中的化学键是共价键查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在含大量Fe3+的溶液中:NH4+、Na+、Cl-、SCN- | |
| B. | 在使酚酞变红的溶液中:Na+、K+、AlO2-、CO32- | |
| C. | 在水电离产生的c(OH-)=1×10-14mol•L-1的溶液中:NH4+、Al3+、SO42-、NO3- | |
| D. | 在pH试纸变深红色的溶液中:K+、Fe2+、Cl-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(OH-)前者大于后者 | |
| B. | 与同浓度的盐酸反应时的反应速率前者大于后者 | |
| C. | 分别加入1L的0.2 mol/L的HNO3 后一定产生4.48LCO2 | |
| D. | 溶液中阳离子浓度相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 室温下测定其pH等于7 | |
| B. | 一个标准大气压下测定其沸点为100℃ | |
| C. | 电解时产生H2、O2的体积比为2:1 | |
| D. | 室温时为无色的液体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com