
| A. | 加入过量NaOH溶液:Na+、AlO2-、OH-、SO42- | |
| B. | 加入过量氨水:NH4+、Al3+、OH-、SO42- | |
| C. | 通入过量SO2:Fe2+、H+、SO32-、SO42- | |
| D. | 加入过量NaClO溶液:Fe2+、Na+、ClO-、SO42- |
分析 加入过量硫酸溶解后过滤,SiO2不反应,则滤液中含有的离子为:Fe3+、Fe2+、Al3+、SO42-、H+,
A.加入过滤氢氧化钠溶液,生成氢氧化铁沉淀,Al3+生成AlO2-;
B.加入氨水,可生成氢氧化铝沉淀;
C.通入过量SO2,与铝离子不反应;
D.NaClO具有强氧化性.
解答 解:加入过量硫酸溶解后过滤,SiO2不反应,则滤液中含有的离子为:Fe3+、Fe2+、Al3+、SO42-、H+,
A.加入过滤氢氧化钠溶液,生成氢氧化铁沉淀,Al3+生成AlO2-,故A正确;
B.加入氨水,可生成氢氧化铝沉淀,溶液不存在Al3+,故B错误;
C.通入过量SO2,与铝离子不反应,溶液中还存在Al3+,故C错误;
D.NaClO具有强氧化性,与Fe2+不能大量共存,故D错误.
故选A.
点评 本题考查离子共存,为高考的高频题,题目难度中等,明确滤液组成为解答关键,试题侧重对学生基础知识的训练和检验,有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力.


科目:高中化学 来源: 题型:解答题
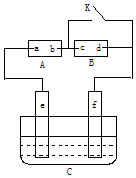 如图A为直流电源,B为浸透饱和氯化钠溶液和酚酞试液的滤纸,C为电镀槽,接通电路后,发现B上的c点显红色,请填空:
如图A为直流电源,B为浸透饱和氯化钠溶液和酚酞试液的滤纸,C为电镀槽,接通电路后,发现B上的c点显红色,请填空:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  该反应过程中的能量变化如图所示 | |
| B. | 该反应条件下,Al的还原性强于Fe | |
| C. | 反应中每生成1 mol Fe转移6×6.02×1023个电子 | |
| D. | 实验室进行该反应时常加入KClO3作催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 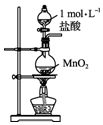 用装置甲制取氯气 | B. | 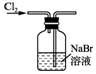 用装置乙氧化溴离子 | ||
| C. | 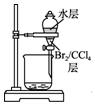 用装置丙分离出溴的CCl4溶液 | D. | 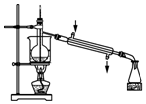 用装置丁获得单质溴 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 煤的干馏和煤的液化均是物理变化 | |
| B. | 天然纤维和合成纤维的主要成分都是纤维素 | |
| C. | 海水淡化的方法有蒸馏法、电渗析法等 | |
| D. | 用活性炭为糖浆脱色和用次氯酸盐漂白纸浆的原理相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 少量SO2 通入漂白粉溶液中:SO2+H2O+Ca2++3C1O-═CaSO4↓+2HC1O+Cl- | |
| B. | 石灰水与过量小苏打溶液反应:Ca2++OH-+HCO3-═CaCO3↓+H2O | |
| C. | FeCl2溶液中通入 C12:Fe2++Cl2═Fe3++2Cl- | |
| D. | NaAlO2 溶液中通入过量CO2:AlO2-+4CO2+2H2O═A13++4HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| t/℃ | 700 | 800 | 830 | 1 000 |
| K | 0.6 | 0.9 | 1.0 | 1.7 |
| A. | 上述生成CO和H2O的反应为放热反应 | |
| B. | 加压、增大H2浓度和加入催化剂都能提高CO2的转化率 | |
| C. | 830℃达平衡后,再充入1.0 mol H2,K值增大,平衡正向移动 | |
| D. | 830℃时反应CO(g)+H2O(g)?CO2(g)+H2(g)的平衡常数为1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com