
amol的下列物质分别与足量的稀硝酸反应(假设还原产物只有一种),消耗硝酸的物质的量均可看作两部分,一部分为作氧化剂的硝酸,另一部分为作酸的(即以硝酸根离子的形式存在于反应后的溶液中维持溶液的电中性),下列各选项中正确的是(单位:mol)( )
①Fe:3a+a ; ②Fe3O4:9a+ ;
③Fe(OH)2:3a+ ; ④FeSO4:a+
A.①②③④ B.只有①② C.只有③④ D.只有①②③
 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案 ABC考王全优卷系列答案
ABC考王全优卷系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
氢气是工业上重要的原料。
(1)氢气用于工业合成氨 N2(g) + 3H2(g) ![]() 2NH3(g);ΔH = -92.2 kJ·mol-1。
2NH3(g);ΔH = -92.2 kJ·mol-1。
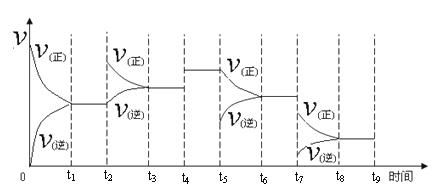
一定温度下,在容积恒定的密闭容器中,一定量的N2和H2反应达到平衡后,改变某一外界条件,反应速率与时间的关系如下图所示,其中t4 ﹑t5 ﹑t7时刻所对应的实验条件改变分别是
t4 t5 t7 。
②温度为T℃时,将2amolH2和amolN2放入0.5L密闭容器中,充分反应后测得N2的转化率为50﹪,此时放出热量46.1 kJ。则该温度下反应的平衡常数为 。
(2)工业上大量的氢气来源于焦炭与水蒸气高温下的反应:
C(s) + H2O(g) ![]() H2(g) + CO(g) △H = +131.3 kJ/mol
H2(g) + CO(g) △H = +131.3 kJ/mol
①该反应在低温下不能自发进行的原因是 。
②恒温,在容积可变的密闭容器中,进行如上可逆反应。一段时间后,下列物理量不发生变化时,能表明该反应已达到平衡状态的有:Ⅰ混合气体的密度;Ⅱ容器内气体的压强;Ⅲ混合气体的总物质的量; ⅣCO物质的量浓度 ( )
A.只有Ⅳ B.只有Ⅰ和Ⅳ C.只有Ⅱ和Ⅲ
D.Ⅰ、Ⅲ和Ⅳ E.都可以
(3)在容积相同的两密闭容器A和B中,保持温度为423K,同时向A、B中分别加入amol及bmol碘化氢(a>b)待反应:2HI(g)![]() H2(g)+I2(g) 达到平衡后,平衡时I2的浓度c(I2)A c(I2)B ;平衡时HI的分解率αA αB ;平衡时H2在混合气体中的体积分数A B (填写“>”“<”“=”)
H2(g)+I2(g) 达到平衡后,平衡时I2的浓度c(I2)A c(I2)B ;平衡时HI的分解率αA αB ;平衡时H2在混合气体中的体积分数A B (填写“>”“<”“=”)
查看答案和解析>>
科目:高中化学 来源: 题型:
填空(有代号的均用代号表示)
(1)下列各组物质(4分)
A、过氧化钠、氧化钙、氟化铜、氧化镁
B、氢气、臭氧、氯气、氮气
C、盐酸、硫酸、硅酸、氢氟酸
D、硫酸氢钠、硫酸钠、硫酸钾、十二水硫酸铝钾
它们的分类依据是:A ;B ;
C ;D ;
(2)下列各物品或设备(2分)
①石英钟表;②陶瓷餐具;③砖瓦;④硅太阳能电池;⑤光导纤维;⑥计算机芯片;⑦石棉;⑧玻璃
Ⅰ、所用材料为SiO2 或用到SiO2的是: ;
Ⅱ、为硅酸盐的是:
(3)下列现象中硫酸所表现出来的性质填写在空白处(4分)
①盛有浓硫酸的烧杯敞口放置一段时间后,质量增加:浓硫酸的
②向蔗糖中加入浓硫酸时,蔗糖变黑,体积膨胀,变成蔬松多孔的海绵状的炭,并有刺激性气味气体产生:浓硫酸的
③在常温下,可以用铁、铝容器盛装冷的浓硫酸:浓硫酸的
④所锌粒放入稀硫酸中,有气体放出:稀硫酸的
(4)把amol/L Cu S04溶液和bmol/L H2S04溶液等体积混合(设混合后体积为混合前两溶液体积之和),则混合液中H+、SO42—、Cu2+ 的物质的量浓度分别是c(H+)= ; c(Cu2+)= ; c(SO42—)=
查看答案和解析>>
科目:高中化学 来源:2011届江苏省盐城中学高三上学期期中考试化学试卷 题型:填空题
氢气是工业上重要的原料。
(1)氢气用于工业合成氨 N2(g) + 3H2(g) 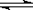 2NH3(g);ΔH =" -92.2" kJ·mol-1。
2NH3(g);ΔH =" -92.2" kJ·mol-1。
① 一定温度下,在容积恒定的密闭容器中,一定量的N2和H2反应达到平衡后,改变某一外界条件,反应速率与时间的关系如下图所示,其中t4 ﹑t5﹑t7时刻所对应的实验条件改变分别是
t4 t5 t7 。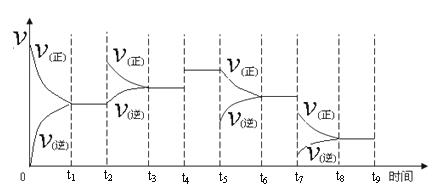
②温度为T℃时,将2amolH2和amolN2放入0.5L密闭容器中,充分反应后测得N2的转化率为50﹪,此时放出热量46.1 kJ。则该温度下反应的平衡常数为 。
(2)工业上大量的氢气来源于焦炭与水蒸气高温下的反应:
C(s) + H2O(g) 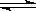 H2(g) + CO(g) △H =" +131.3" kJ/mol
H2(g) + CO(g) △H =" +131.3" kJ/mol
①该反应在低温下不能自发进行的原因是 。
②恒温,在容积可变的密闭容器中,进行如上可逆反应。一段时间后,下列物理量不发生变化时,能表明该反应已达到平衡状态的有:Ⅰ混合气体的密度;Ⅱ容器内气体的压强;Ⅲ混合气体的总物质的量; ⅣCO物质的量浓度 ( )
A.只有Ⅳ B.只有Ⅰ和Ⅳ C.只有Ⅱ和Ⅲ
D.Ⅰ、Ⅲ和Ⅳ E.都可以
(3)在容积相同的两密闭容器A和B中,保持温度为423K,同时向A、B中分别加入amol及bmol碘化氢(a>b)待反应:2HI(g)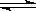 H2(g)+I2(g) 达到平衡后,平衡时I2的浓度c(I2)A c(I2)B ;平衡时HI的分解率αA αB ;平衡时H2在混合气体中的体积分数A B (填写“>”“<”“=”)
H2(g)+I2(g) 达到平衡后,平衡时I2的浓度c(I2)A c(I2)B ;平衡时HI的分解率αA αB ;平衡时H2在混合气体中的体积分数A B (填写“>”“<”“=”)
查看答案和解析>>
科目:高中化学 来源:2010-2011学年江苏省高三上学期期中考试化学试卷 题型:填空题
氢气是工业上重要的原料。
(1)氢气用于工业合成氨 N2(g)
+ 3H2(g) 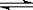 2NH3(g);ΔH
= -92.2 kJ·mol-1。
2NH3(g);ΔH
= -92.2 kJ·mol-1。
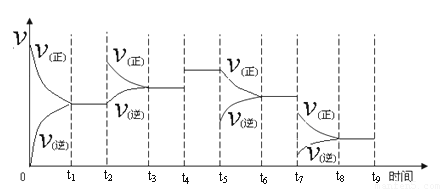
① 一定温度下,在容积恒定的密闭容器中,一定量的N2和H2反应达到平衡后,改变某一外界条件,反应速率与时间的关系如下图所示,其中t4 ﹑t5 ﹑t7时刻所对应的实验条件改变分别是
t4 t5 t7 。
②温度为T℃时,将2amolH2和amolN2放入0.5L密闭容器中,充分反应后测得N2的转化率为50﹪,此时放出热量46.1 kJ。则该温度下反应的平衡常数为 。
(2)工业上大量的氢气来源于焦炭与水蒸气高温下的反应:
C(s) + H2O(g) 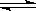 H2(g)
+ CO(g) △H = +131.3 kJ/mol
H2(g)
+ CO(g) △H = +131.3 kJ/mol
①该反应在低温下不能自发进行的原因是 。
②恒温,在容积可变的密闭容器中,进行如上可逆反应。一段时间后,下列物理量不发生变化时,能表明该反应已达到平衡状态的有:Ⅰ混合气体的密度;Ⅱ容器内气体的压强;Ⅲ混合气体的总物质的量; ⅣCO物质的量浓度 ( )
A.只有Ⅳ B.只有Ⅰ和Ⅳ C.只有Ⅱ和Ⅲ
D.Ⅰ、Ⅲ和Ⅳ E.都可以
(3)在容积相同的两密闭容器A和B中,保持温度为423K,同时向A、B中分别加入amol及bmol碘化氢(a>b)待反应:2HI(g)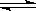 H2(g)+I2(g) 达到平衡后,平衡时I2的浓度c(I2)A
c(I2)B ;平衡时HI的分解率αA αB
;平衡时H2在混合气体中的体积分数A B (填写“>”“<”“=”)
H2(g)+I2(g) 达到平衡后,平衡时I2的浓度c(I2)A
c(I2)B ;平衡时HI的分解率αA αB
;平衡时H2在混合气体中的体积分数A B (填写“>”“<”“=”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com