
【题目】下列反应中符合下列图象的是( ) 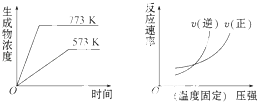
A.N2(g)+3H2(g)2NH5(g)△H=﹣Q1kJmol﹣1(Q1>0)
B.2SO5(g)2SO2(g)+O2(g)△H=+Q2kJmol﹣1(Q2>0)
C.4NH5(g)+5O2(g)4NO(g)+6H2O(g)△H=﹣Q3kJmol﹣1(Q3>0)
D.H2(g)+CO(g)C(g)+H2O(g)△H=+Q4kJmol﹣1(Q4>0)
【答案】B
【解析】解:由图可知温度越高,生成物浓度越大,则升高温度平衡正移,该反应为吸热反应,由第二个图可知增大压强逆速率增大的快,则增大压强平衡逆移,则该反应正方向为体积增大的方向,
A.N2(g)+3H2(g)2NH5(g)△H=﹣Q1kJmol﹣1(Q1>0)该反应为放热反应,不符合,故A不选;
B.2SO5(g)2SO2(g)+O2(g)△H=+Q2kJmol﹣1(Q2>0)该反应为吸热反应,反应正方向为体积增大的方向,符合题意,故B选;
C.4NH5(g)+5O2(g)4NO(g)+6H2O(g)△H=﹣Q3kJmol﹣1(Q3>0)该反应为放热反应,不符合题意,故C不选;
DH2(g)+CO(g)C(g)+H2O(g)△H=+Q4kJmol﹣1(Q4>0)该反应为吸热反应,反应正方向为体积减小的方向,故D不选.
故选B.
【考点精析】通过灵活运用反应热和焓变,掌握在化学反应中放出或吸收的热量,通常叫反应热即可以解答此题.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】某学习小组在实验室中利用下图装置(夹持装置略去)测定某铁硫化物(FexSy)的组成,并探究反应后D装置所得溶液中含硫化合物的组成。

实验步骤:
步骤I如图连接装置,检查装置气密性,装入药品;
步骤II旋开滴液漏斗活塞与旋塞,并点燃酒精喷灯;
步骤III当硬质玻璃管中固体质量不再改变时,停止加热,继续向烧瓶中滴水一段时间
步骤IV实验结束后,将D中所得溶液加水配制成250mL溶液;
……
请回答:
(1)步骤III中,停止加热后还需继续向烧瓶中滴水一段时间,其目的为___________________。
(2)在C、D装置之间不需要防倒吸装置的理由是_______________________________________。
(3)步骤IV中配制溶液时所需的玻璃仪器除玻璃棒和烧杯外,还有_____________________。
(4)取25.00mL步骤IV 中所配溶液,加入足量的双氧水,再加入足量盐酸酸化的BaCl2溶液,将所得沉淀过滤、洗涤、干燥,称其质量为4.66g。则FexSy的化学式为________________。
(5)有同学认为可将装置D改为装有足量碱石灰的干燥管,通过测定反应前后干燥管的增重来计算硫元素的含量。你认为此方案____(填“是”或“否”)合理,原因为_____________________。
(6)反应后D装置所得溶液中除含有Na2SO4外,还可能含有Na2SO3。现用滴定法测定溶液中Na2SO3的含量。可供选择的试剂:①0.1000mol/LKMnO4酸性溶液;②0.1000mol/LH2O2溶液;③0.1000mol/LKI淀粉溶液;④0.1000 mol/LBaCl2溶液;⑤0.1000mol/LHCl溶液。
①所选试剂应装在_____(填“酸式”或“碱式”) 滴定管中。
②所利用的反应原理为___________________________________(用离子方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是自来水表的常见安装方式.下列有关说法不正确的是( ) 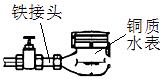
A.发生腐蚀过程中,电子从接头流向水表
B.腐蚀时,铁接头发生的是还原反应
C.腐蚀时铜质水表发生的电极反应为:2H2O+O2+4e﹣═4OH﹣
D.腐蚀过程还涉及到反应:4Fe(OH)2+2H2O+O2═4Fe(OH)3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表中根据实验操作和现象所得出的结论正确的是( )
选项 | 实验操作 | 实验现象 | 实验结论 |
A | 蘸有浓氨水的玻璃棒靠近X | 有白烟产生 | X一定是浓盐酸 |
B | KIO3溶液中加入HI溶液,并加入淀粉 | 溶液变蓝色 | KIO3的氧化性比I2的强 |
C | 强酸性溶液Y中加入Ba(NO3)2溶液,静置后再加入KSCN溶液 | 先有白色沉淀,后溶液又变红 | Y中一定含有SO |
D | C2H5OH与浓硫酸混合后加热到170 ℃ | 制得的气体使酸性KMnO4溶液褪色 | 一定是制得的乙烯使酸性KMnO4溶液褪色 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.下表为元素周期表的一部分,请按要求回答问题:
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | ① | ② | ③ | ④ | ⑤ | |||
3 | ⑥ | ⑦ | ⑧ | ⑨ |
(1)表中元素______的非金属性最强,元素_____的金属性最强(填元素符号)。
(2)表中元素④、⑨形成的氢化物的稳定性顺序为_____>______(填化学式)。
(3)表中元素③、④、⑥、⑦的原子半径大小为____>____>___>___(填元素符号)。
Ⅱ.A、B、W、D、E为短周期元素,且原子序数依次增大,五种元素核内质子数之和为39,B、W同周期,A、D同主族,A、W能形成两种液态化合物A2W和A2W2,E元素的周期序数与主族序数相等。
(1)A2W的电子式为________。(2) E元素在周期表中的位置为_______ 。
(3)W、D、E三种元素的简单离子半径由小到大的顺序为_______(填离子符号)。
(4)在一定条件下,D元素的单质能与A元素的单质化合生成DA,DA能与水反应放氢气,则其化学方程式为_______
(5)若要比较D和E的金属性强弱,下列实验方法可行的是_______。
a.将D单质置于E的盐溶液中,若单质D不能置换出单质E,说明D的金属性弱
b.将少量D、E的单质分别投入到水中,若D反应而E不反应,说明D的金属性强
C.比较相同条件下D和E的最高价氧化物对应水化物的溶解性若前者比后者溶解度大,说明D的金属性强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氟化硼是平面正三角形,因此是非极性分子,推断三氯甲烷(碳原子位于分子结构中心)的结构和分子的极性情况是( )
A. 四面体,极性分子 B. 平面三角形,非极性分子
C. 正四面体,非极性分子 D. 平面三角形,极性分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原子序数依次增大的A、B、C、D、E、F六种元素。其中A的基态原子有3个不同的能级,各能级中的电子数相等;C的基态原子2p能级上的未成对电子数与A原子的相同;D为它所在周期中原子半径最大的主族元素;E和C位于同一主族,F的原子序数为29。
(1)F基态原子的核外电子排布式为______________________。
(2)在A、B、C三种元素中,第一电离能由小到大的顺序是___________(用元素符号回答)。
(3)元素B的简单气态氢化物的沸点___________(填“高于”或“低于”)元素A的简单气态氢化物的沸点,其主要原因是______________________。
(4)由A、B、C形成的离子CAB与AC2互为等电子体,则CAB的结构式为___________。
(5)由B、C、D三种元素形成的化合物晶体的晶胞如图所示,则该化合物的化学式为___________。

(6)FC在加热条件下容易转化为F2C,从原子结构的角度解释原因______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com