
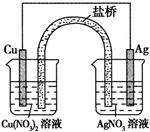
 用铜片、银片、CuSO4溶液、AgNO3溶液、导线和盐桥(装有琼脂-KNO3的U形管)构成一个原电池(如图).以下有关该原电池的叙述正确的是( )
用铜片、银片、CuSO4溶液、AgNO3溶液、导线和盐桥(装有琼脂-KNO3的U形管)构成一个原电池(如图).以下有关该原电池的叙述正确的是( )

 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案科目:高中化学 来源: 题型:
 (1)实验证明能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是
(1)实验证明能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是
|
|
|
| O | - 3 |
| ||
| ||
查看答案和解析>>
科目:高中化学 来源:2012届安徽省高二下学期期中考试化学试卷 题型:选择题
用铜片、银片、CuSO4溶液、AgNO3溶液、导线和盐桥(装有琼脂—KNO3的U形管)构成一个原电池(如图)。以下有关该原电池的叙述正确的是

①在外电路中,电子由铜电极流向银电极
②正极反应为:Ag++e-=Ag
③盐桥中K+移向CuSO4溶液
④将铜片浸入AgNO3溶液中发生的化学反应与该原电池总反应相同
A.①② B.①②④ C.①②③ D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
用铜片、银片、CuSO4溶液、AgNO3溶液、导线和盐桥(装有琼脂—KNO3的U形管)构成一个原电池(如右图)。以下有关该原电池的叙述正确的是
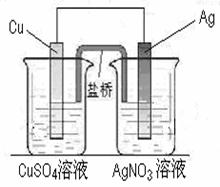 ①在外电路中,电子由铜电极流向银电极
①在外电路中,电子由铜电极流向银电极
②正极反应为:Ag++e-=Ag
③盐桥中K+移向CuSO4溶液
④将铜片浸入AgNO3溶液中发生的化学反应与该原电池总反应相同
A.①② B.①②④
C.①②③ D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
用铜片、银片、CuSO4溶液、AgNO3溶液、导线和盐桥(装有琼脂—KNO3的U形管)构成一个原电池(如图)。以下有关该原电池的叙述正确的是
①在外电路中,电子由铜电极流向银电极
②正极反应为:Ag++e-=Ag
③盐桥中K+移向CuSO4溶液
④将铜片浸入AgNO3溶液中发生的化学反应与该原电池总反应相同
A.①② B.①②④ C.①②③ D.①②③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com