
【题目】下列物质混合后不能发生离子反应的是( )
A. 硫酸溶液与食盐水 B. 硫酸铜溶液与氢氧化钠溶液
C. 锌片与稀硫酸 D. Cl2通入氢氧化钠溶液中
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案科目:高中化学 来源: 题型:
【题目】下列物质按纯净物、混合物、强电解质和非电解质顺序排列的是( )
A. 单甘油酯、混甘油酯、苛性钾、H2S、
B. 胆矾、漂白粉、硫酸钠、次氯酸
C. 明矾、水煤气、盐酸、铜
D. 冰醋酸、福尔马林、硫酸钡、乙醇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以某含铜矿石[主要成分为FeCu4SiO5(OH)4,含少量SiO2、CuCO3]为原料,制备CuSO4·5H2O的流程如下:
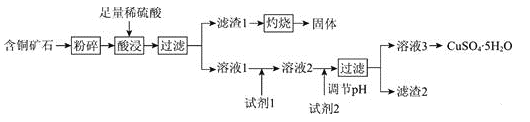
已知:
ⅰ.溶液中离子浓度小于等于1.0×10-5mol·L-1时,认为该离子沉淀完全。
ⅱ.相关试剂成分和价格如表1所示。
ⅲ.25℃时,该流程中金属离子生成氢氧化物时,开始沉淀和沉淀完全的pH如表2所示。
表1
试剂 | 成分 | 价格/(元·吨-1) |
漂白液 | 含25.2%NaClO | 450 |
双氧水 | 含30%H2O2 | 2400 |
浓硝酸 | 含98%HNO3 | 1500 |
表2
氢氧化物 | 开始沉淀的pH | 沉淀完全的pH |
Fe(OH)2 | 7.6 | 9.6 |
Fe(OH)3 | 2.7 | 3.7 |
Cu(OH)2 | 4.0 | 6.5 |
请回答:
(1)FeCu4SiO5(OH)4用氧化物的形式可表示为________。
(2)结合题中信息,所选用的试剂1的名称为________;加入该试剂时,所发生反应的离子方程式为________。
(3)加入试剂2,需调节溶液的pH的合理范围为________。试剂2可以选择下列物质中的________(填字母)。
A.Cu B.CuO
C.Cu(OH)2 D.Fe
(4)25℃时,Cu(OH)2的溶度积常数Ksp[Cu(OH)2]=________。
(5)CuSO4·5H2O溶液可用于电解精炼铜。电解精炼铜时,导线中通过9.632×104C的电量时,理论上阴极质量增加________g。(已知:1个电子的电量为1.6×10-19C)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下面的反应路线及所给信息,回答下列问题:
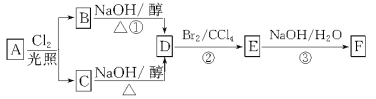
A在氧气中充分燃烧可以产生88 g CO2和45 g H2O。A的分子式是_______。
(2)B和C均为一氯代烃,它们的名称(系统命名)分别为_________________。
(3)D的结构简式________________,D中碳原子是否都处于同一平面?________。
(4)E的同分异构体的结构简式是___________________________。
(5)①、②、③的反应类型依次是_________________________。
(6)写出②、③的反应化学方程式_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关水解原理的应用,下列说法正确的是
A.将NaHCO3溶液蒸干并灼烧时,HCO3-+H2O![]() H2CO3+OH-向正向移动,最后可以得到NaOH固体
H2CO3+OH-向正向移动,最后可以得到NaOH固体
B.MgSO4酸性溶液中含有杂质离子Fe2+时,可以先加人氯水将Fe2+氧化成Fe3+,再加入MgO除去杂质
C.为抑制离子的水解,在配制SnCl2溶液时,可以加入适量稀硫酸加以酸化
D.用MgCl2 6H2O制取无水MgCl2时,需要在HCl气流中加热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列变化中,气体仅被还原的是
A. 二氧化碳使Na2O2固体变白 B. 氯气使KBr溶液变黄
C. 二氧化氮溶于水 D. 氨气使AlCl3溶液产生白色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知M2O7x-+3S2-+14H+=2M3++3S↓+7H2O,则M2O7x-中的M的化合价为
A.+2价 B.+3价 C.+4价 D.+6价
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝与过量的稀盐酸反应,为了加快反应速率,但是又不影响生成的氢气总量,可以采取的措施是( )
A. 加入适量的铝粉 B. 加入适量的水
C. 加入少量的硫酸铜溶液 D. 加入浓度较大的盐酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com