
| A. | 绿色植物光合作用过程中是由太阳能转变成化学能 | |
| B. | 研制乙醇汽油技术,可降低机动车辆尾气中有害气体的排放 | |
| C. | 煤、石油、天然气属于可再生能源 | |
| D. | 利用太阳能等清洁能源代替化石燃料,有利于节约资源、保护环境 |
分析 A、光合作用时,太阳能转化为化学能;
B、乙醇汽油是一种由粮食及各种植物纤维加工成的燃料乙醇和普通汽油按一定比例混配形成替代能源;
C、煤、石油和天然气是化石燃料;
D、太阳能等清洁能源的利用能大大减少化石燃料的使用.
解答 解:A、绿色植物进行光合作用时,太阳能转化为化学能在生物体内储存,故A正确;
B、可以有效改善油品的性能和质量,降低一氧化碳、碳氢化合物等主要污染物排放.它不影响汽车的行驶性能,还减少有害气体的排放量,故B正确;
C、煤、石油和天然气是化石燃料,短期内不能再生,是不可再生能源,故C错误;
D、太阳能等清洁能源的利用能大大减少化石燃料的使用,减少有毒气体的排放、二氧化碳的排放,减少环境污染,故D正确;
故选C.
点评 本题考查了生活环境污染及治理,明确物质的性质是解本题关键,根据物质的性质来分析解答,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
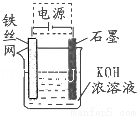 铁及其化合物在生产、生活中有广泛应用.请回答下列问题:
铁及其化合物在生产、生活中有广泛应用.请回答下列问题:| 温度/℃ | 1000 | 1115 | 1300 |
| 平衡常数 | 4.0 | 3.7 | 3.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C的生成速率与C的分解速率相等 | |
| B. | A、B、C的分子数之比是1:3:2 | |
| C. | 单位时间内生成n molA,同时生成3n mol B | |
| D. | A、B、C的浓度相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Mg+2H2O═Mg(OH)2+H2↑ | B. | 2H2O$\frac{\underline{\;电解\;}}{\;}$2H2↑+O2↑ | ||
| C. | 2F2+2H2O═O2+4HF | D. | 3NO2+H2O═2HNO3+NO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙酸根离子的结构式: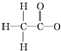 | |
| B. | CO2分子的球棍模型: | |
| C. | 3-甲基-1-丁烯的结构简式:(CH3)2CHCH=CH2 | |
| D. | 醛基的电子式为 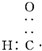 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
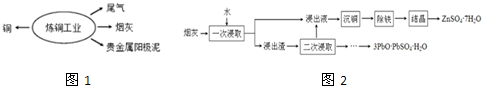
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 碳碳间以单键结合,碳原子剩余价键全部与氢原子结合的烃一定是饱和链烃 | |
| B. | 分子组成符合CnH2n+2的烃一定是烷烃 | |
| C. | 烷烃分子中所有的碳原子均在同一条直线上 | |
| D. | 甲烷和异丁烷互为同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molO2的质量为32g/mol | |
| B. | 1mol物质的质量等于该物质的相对分子质量 | |
| C. | SO42-的摩尔质量为96g/mol | |
| D. | 1mol CO2的体积是22.4L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com