
| A. | I-、ClO-、NO3-、H+ | B. | Fe3+、Cu2+、SO42-、Cl- | ||
| C. | H+、K+、AlO2-、HSO3- | D. | Ca2+、Na+、SO42-、CO32- |
科目:高中化学 来源: 题型:选择题
| A. | 稀释浓硫酸时,应将蒸馏水沿玻璃棒缓慢注入浓硫酸中 | |
| B. | 配制溶液时,若加水超过容量瓶刻度线,应用胶头滴管将多余溶液吸出 | |
| C. | 检验某溶液是否含有SO42-时,应取少量该溶液,依次加入BaCl2溶液和稀盐酸 | |
| D. | 用分液的方法分离汽油和氯化钠溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
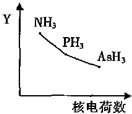 氮族元素氢化物RH3(NH3、PH3、AsH3)的某种性质随R的核电荷数的变化趋势如图所示,则Y轴可表示的是( )
氮族元素氢化物RH3(NH3、PH3、AsH3)的某种性质随R的核电荷数的变化趋势如图所示,则Y轴可表示的是( )| A. | 相对分子质量 | B. | 稳定性 | C. | 沸点 | D. | R-H键长 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
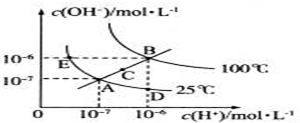
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol/L | B. | 0.2mol/L | C. | 0.4mol/L | D. | 0.8mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氟酸、食盐水 | B. | 氨水、碘酒 | C. | 石灰水、硝酸 | D. | 稀硫酸、食醋 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | PM2.5是指大气中直径小于或等于2.5微米的颗粒物,也称为可入肺颗粒物,分散在空气中不可能形成胶体 | |
| B. | 生活中常见的石英玻璃、普通玻璃、钢化玻璃都属于硅酸盐产品 | |
| C. | 食品添加剂对人体均有益,可随意使用 | |
| D. | 洪涝、地震灾区灾后可用石灰消毒,是利用石灰可使蛋白质变性的性质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | PH=12的溶液:NH4+、Na+、Cl-、HCO3- | |
| B. | 能使pH试纸变红色的溶液:Na+、Al3+、NO3-、SO42- | |
| C. | 含有大量Fe3+的溶液:SCN-、I-、K+、Br- | |
| D. | 澄清透明的无色溶液:ClO-、MnO4-、Al3+、SO42- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com