
分析 (1)ClO2为氧化物,类似二氧化碳,O为-2价,化合物中正负化合价的代数和为0;
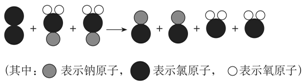
(2)由图可知,氯气与NaClO2以物质的量为1:2反应.
解答 解:(1)ClO2的名称为二氧化氯,氯元素的化合价为0-(-2)×2=+4,故答案为:二氧化氯;+4;
(2)由图可知,氯气与NaClO2以物质的量为1:2反应,生成等物质的量的氯化钠、二氧化氯,则反应为Cl2+2NaClO2═2NaCl+2ClO2,故答案为:Cl2+2NaClO2═2NaCl+2ClO2.
点评 本题考查含氯物质的性质,为高频考点,把握物质的名称、元素的化合价、发生的反应为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 焦炭在高温下还原二氧化硅制粗硅 | B. | 电解熔融氧化铝制金属铝 | ||
| C. | 二氧化碳和氢氧化钠反应制碳酸钠 | D. | 氯气与石灰乳反应制漂白粉 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Mg2+、Na+、Cl-、SO42- | B. | K+、Na+、NO3-、MnO4- | ||
| C. | K+、Na十、Cl-、Cu2+ | D. | Na十、Ba2+、OH-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化钠和氯化铯晶体中,阳离子的配位数均为6 | |
| B. | 金刚石为三维网状结构,由碳原子以sp3杂化轨道形成共价键 | |
| C. | 金属钠的晶体采用体心立方堆积,每个晶胞含2个原子,配位数为8 | |
| D. | 干冰晶体中,每个CO2分子周围紧邻12个CO2分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 破坏生成物全部化学键所需要的能量大于破坏反应物全部化学键所需要的能量,该反应为吸热反应 | |
| B. | 任何酸与碱发生中和反应生成1 mol H2O的过程中,能量变化均相同 | |
| C. | 已知:①2H2(g)+O2(g)=2H2O(g)△H1,②2H2(g)+O2 (g)=2H2O(1)△H2,则△H1<△H2 | |
| D. | 已知:①C(s,石墨)+O2 (g)=CO2(g)△H=-393.5kJ•mol-1, ②C(s,金刚石)+O2(g)=CO2 (g)△H=-395.0 kJ•mol-1则C(s,石墨)=C(s,金刚石)△H=+1.5 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②④⑤⑥ | B. | ①②④ | C. | ②④⑥ | D. | ②⑥ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com