
【题目】把SO2通入Fe(NO3)3溶液中,溶液由黄色变为浅绿色,但立即又变为黄色,此时若滴入BaCl2溶液,则会产生白色沉淀。在上述一系列变化过程中,最终被还原的是( )
A.SO2 B.NO3- C.Fe3+ D.Fe2+
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案科目:高中化学 来源: 题型:
【题目】下列物质中肯定为纯净物的是
A. 只由一种元素组成的物质
B. 只由一种原子组成的物质
C. 只由一种分子组成的物质
D. 只由一种元素的阳离子与另一种元素的阴离子组成的物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式书写正确的
A. 甲烷的燃烧热为-890 kJ/mol,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+ 2H2O(g)△H=-890 kJ/mol
B. 在一定条件下将1 molSO2和0.5molO2置于密闭容器中充分反应,放出热量79.2kJ,则反应的热化学方程式为:2SO2(g)+O2(g)![]() 2SO3(g) △H=-158.4kJ·mol-1
2SO3(g) △H=-158.4kJ·mol-1
C. NaOH(s)+1/2H2SO4(浓)=1/2Na2SO4(aq)+H2O(l) △H=-57.3kJ·mol-1
D. 2.00gC2H2气体完全燃烧生成液态水和二氧化碳气体放出99.6kJ的热量,该反应的热化学方程式为:2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) △H=-2589.6kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜是一种重要的战略物资,以黄铜矿(主要成分是CuFeS2)为主要原料生产铜、铁红、单质硫时,原料的综合利用率较高,其主要流程如图所示(己知Na[CuCl2]的电离方程式为:Na[CuCl2]=Na++[CuCl2]-):
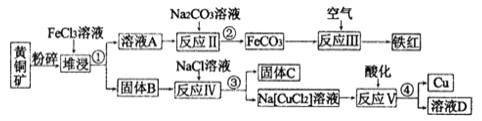
(1)流程中粉碎的目的是_____________,操作①、②、③、④的目的相同,在实验中这种操作的名称是____________。
(2)铁红的重要用途:__________________,固体B中含有两种产物,一种是单质C、另一种是原子个数比为1:l 的一种金属的低价态盐,写出堆浸时反应的化学方程式:________。
(3)反应V的离子方程式:___________________。
(4)此方法中得到的铜纯度不能满足某些生产的需要,需要利用电解法进行提纯。若用如图所示的装置进行电解精炼,则乙中溶液的溶质是_________,e电极上的电极反应式为_____。
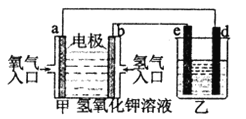
若当电路中有2mol电子通过时,乙中某个电极质量减轻了63.92g,则粗铜的纯度为(假设杂质只有铁且精炼时铜与铁的放电比例与混合物比例相同,计算时用%表示保留一位小数)____________(已知相对原子质量:Fe 56 Cu 64 )。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高氯酸、硫酸、硝酸和盐酸都是强酸,其酸性在水溶液中差别不大。以下是某温度下这四种酸在冰醋酸中的电离常数:
酸 | HClO4 | H2SO4 | HCl | HNO3 |
Ka | 1.6×10-5 | 6.3×10-9 | 1.6×10-9 | 4.2×10-10 |
从以上表格中判断以下说法中不正确的是
A.在冰醋酸中硫酸的电离方程式为H2SO4===2H++SO![]()
B.在冰醋酸中高氯酸是这四种酸中最强的酸
C.在冰醋酸中这四种酸都没有完全电离
D.水对于这四种酸的强弱没有区分能力,但醋酸可以区别这四种酸的强弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2.1g平均相对分子质量为7.2的CO与H2组成的混合气体与足量的O2充分燃烧后,立即通入足量的Na2O2固体中,固体的质量增加
A.2.1g B.3.6g C.7.2g D.不可求
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将标准状况下的11.2L氨气溶于100mL水中,得到密度为0.868gcm-3的氨水。 (1)该气体的物质的量=_______mol;所得氨水的物质的量浓度= _______molL-1。 (2)若取上述氨水30.0mL与70.0mL2.00molL-1的AlCl3溶液相混合,产生白色沉淀的质量是___________g。
(3)若取一定体积浓度为5.00molL-1的NaOH溶液与50.0mL2.00molL-1的AlCl3溶液相混合,有白色沉淀产生,测得溶液中铝元素与沉淀中铝元素质量相等,则NaOH溶液的体积为____________mL。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com