
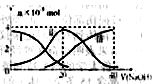



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ��ʴ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��1��10��1010��109 | B��1��5��5��109��5��109 |
| C��1��20��1010��109 | D��1��10 ��104��109 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����Ȼ����ʯ�͡���ˮ������������Ϊһ����Դ |
| B�������Ƿ������绹�ǻ������磬���ǽ���ѧ��ת��Ϊ���� |
| C��PM 2.5���е�Ǧ���ӡ�����������ȶ������к���Ԫ�ؾ��ǽ���Ԫ�� |
| D����չ��̼���á�ѭ�����ã��ƹ�����̫���ܡ����ܵij�������ϵͳ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| | �� | �� | �� | �� |
| pH | 11 | 11 | 3 | 3 |
| ��Һ | ��ˮ | ����������Һ | ���� | ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
A��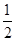 N2H4(g)�� N2H4(g)��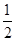 O2(g)=== O2(g)===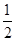 N2(g)��H2O(g) ��H����267 kJ��mol��1 N2(g)��H2O(g) ��H����267 kJ��mol��1 |
| B��N2H4(g)��O2(g)===N2(g)��2H2O(l) ��H����133.5 kJ��mol��1 |
| C��N2H4(g)��O2(g)===N2(g)��2H2O(g) ��H����534 kJ��mol��1 |
| D��N2H4(g)��O2(g)===N2(g)��2H2O(g) ��H����534 kJ��mol��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ��ʴ���
 a��c(Na+)= c(H2S)+c(HS?)+2c(S2?)
a��c(Na+)= c(H2S)+c(HS?)+2c(S2?) ��4����ҵ������·ѭ����������������Ĺ�����������ͼ��ʾ��
��4����ҵ������·ѭ����������������Ĺ�����������ͼ��ʾ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��

| A������������������c(H��)��c(OH��)��Kw |
| B��M��������������c(H��)��c(OH��) |
| C��ͼ��T1��T2 |
| D��XZ������������pH��7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
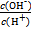 =1��10-12,����˵������ȷ����
=1��10-12,����˵������ȷ����| A����Һ����ˮ�������c(H+)=1��10-10 mol��L-1 |
B����Һ�д���HA H++A- H++A- |
| C����0.1 mol��L-1 NaOH��Һ�������Ϻ�������ҺΪ���� |
| D��ԭ��Һ�м���һ����NaA������ˮϡ��,��Һ��c(OH-)������ |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com