
| A.Ksp反映了物质在水中的溶解能力,但不可以直接根据Ksp的数值大小比较电解质在水中的溶解能力大小 |
| B.乙醇汽油是多种烃的混合物 |
| C.非金属元素的原子间只形成共价键,金属元素的原子与非金属元素的原子间只形成离子键 |
| D.我国规定自 2008 年 6 月 1 日起,商家不得无偿提供塑料袋,目的是降低生产成本 |
 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案科目:高中化学 来源:不详 题型:单选题
| A.pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,滴入石蕊溶液呈蓝色 |
| B.该溶液由等物质的量浓度、等体积的NaOH溶液和CH3COOH溶液混合而成 |
| C.在NaOH溶液中加入一定量的CH3COOH溶液,只有当溶液中离子浓度满足: c(Na+)>c(CH3COO-)>c(OH-)>c(H+)时,才符合题意。 |
| D.加入适量氨水,c(CH3COO-)一定大于c(Na+)、c(NH4+)之和 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.5.0×10—3mol/L | B.1.0×10—7mol/L |
| C.1.1×10—12mol/L | D.2.2×10—13mol/L |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.pH=7的溶液 |
| B.c(NH4+)=c(Cl-)的NH4Cl和氨水的混合溶液 |
| C.PH=2的CH3COOH和PH=12的NaOH溶液等体积混合 |
| D.CH3COONa溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
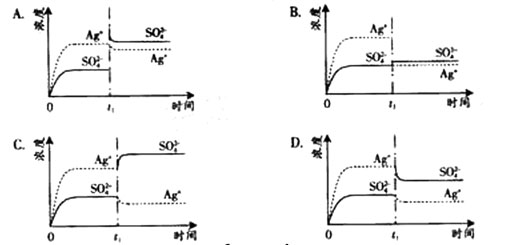
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.K+、Ba2+、Cl-、NO3- | B.Fe3+、Cu2+、Cl-、HCO3- |
| C.K+、Na+、SO32-、SO42- | D.Ca2+、Al3+、H+、NO3- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Ag+、Na+、NO3-、I- | B.H+、Mg2+、SO42-、F- |
| C.K+、Mg2+、SO42-、NO3- | D.K+、Fe3+、NO3-、SO42- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Na+、Ag+、NO3-、MnO4- | B.Fe3+、H+、I-、HCO3- |
| C.K+、Na+、NO3-、ClO- | D.NH4+、Mg2+、SO42-、OH- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com