

| A.稀释后x溶液中水的电离程度比y溶液中水电离程度小 |
| B.若x、y是一元碱,则等物质的量浓度的y的硝酸盐溶液的pH比x的硝酸盐溶液大 |
| C.若x、y都是弱碱,则a的值一定大于9 |
| D.完全中和x、y两溶液时,消耗同浓度稀硫酸的体积V(x)>V(y) |
 优等生题库系列答案
优等生题库系列答案 53天天练系列答案
53天天练系列答案科目:高中化学 来源:不详 题型:填空题
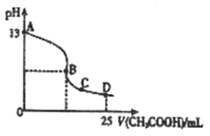
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 H="-483.6" kJ/mol
H="-483.6" kJ/mol H="-57.3" kJ/mol
H="-57.3" kJ/mol| A.H2的燃烧热为285.8 kJ/mol |
B.H2和O2反应生成液态水时的热化学方程式为H2(g) +1/2O2(g)=H2O(l) H="-571.6" kJ/mol H="-571.6" kJ/mol |
| C.稀硫酸与稀NaOH溶液反应的中和热为-57.3 kJ |
| D.稀醋酸与稀NaOH溶液反应生成1mol水,放出57.3kJ热量 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.酸溶于水后能促进水的电离,碱溶于水后能抑制水的电离。 |
| B.强酸溶于水后能抑制水的电离,弱酸溶于水后能促进水的电离。 |
| C.任何条件下,只要c(H+)>c(OH-),溶液就一定显酸性。 |
| D.任何条件下,只要pH>7,溶液就一定显碱性。 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.20:1 | B.1:20 | C.10:1 | D.1:10 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.0.03mol/L | B.0.3mol/L | C.0.05mol/L | D.0.04mol/L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com