
催化剂是化工技术的核心,绝大多数的化工生产均需采用催化工艺。
(1)人们常用催化剂来选择反应进行的方向。下左图所示为一定条件下1mol CH3OH与O2发生反应时,生成CO、CO2或HCHO的能量变化图[反应物O2(g)和生成物H2O(g)略去]。
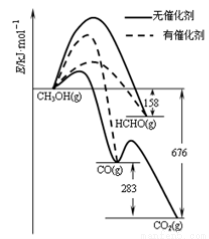
①在有催化剂作用下,CH3OH与O2 反应主要生成 (填“CO、CO2、HCHO”);
②2HCHO(g)+O2(g)=2CO(g)+2H2O(g) △H= 。
(2)一种以铜作催化剂脱硫有如下两个过程:
①在铜的作用下完成工业尾气中SO2的部分催化氧化,所发生反应为:
2SO2+2n Cu+(n+1)O2+(2-2 n) H2O=2n CuSO4+(2-2n) H2SO4
从环境保护的角度看,催化脱硫的意义为 ;每吸收标准状况下11.2L SO2,被SO2还原的O2的质量为 g。
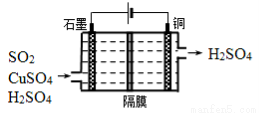
②利用下图所示电化学装置吸收另一部分SO2,并完成Cu的再生。写出装置内所发生反应的离子方程式 。
(1) HCHO :-470kj/mol
(2)① 防止形成酸雨 (2分) 8 (2分)
② SO2+2H2O+Cu2+ 4H++SO42―+Cu (2分,条件不写扣1分,未配平扣1分)
4H++SO42―+Cu (2分,条件不写扣1分,未配平扣1分)
【解析】
试题分析:
(1)据图像可以看出转化成甲醛时的活化能最低,使用催化剂时主要产物为甲醛
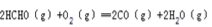 该反应为放热反应
该反应为放热反应
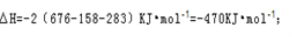
(2)1.脱硫可以减少二氧化硫的排放量,防止酸雨的形成
 推测出m=8g
推测出m=8g
2.分析图中电解装置,可知左边石墨是电解池的阳极,右边是阴极。阳极放电的物质二氧化碳,失去电子生成硫酸根离子,电极反应式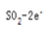
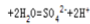 ,阴极放电的物质是铜离子,得到电子被还原成 单质铜,电极反应式为
,阴极放电的物质是铜离子,得到电子被还原成 单质铜,电极反应式为 ,将上述两电极的电极反应式得
,将上述两电极的电极反应式得
考点:考查反应热的计算,盖斯定律,二氧化硫的污染和治理,电解原理的相关知识点


科目:高中化学 来源:2013-2014浙江省高二下学期期末考试化学试卷(解析版) 题型:填空题
已知A的分子式为C3H4O2,下图是A~H间相互转化的关系图,其中F中含有一个七元环;H是一种高分子化合物。(提示:羟基与双键碳原子相连的醇不存在;同一个碳原子上连有2个或多个羟基的多元醇不存在)
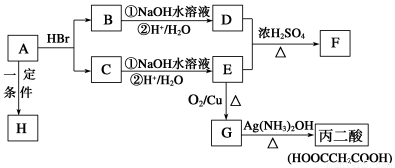
请填写下列空白:
(1)A中含有的官能团有(写名称)_________ _________。
(2)请写出下列有机物的结构简式:C_______________;F______________
(3)请指出下列反应的反应类型:A→B____________;C→E___________。
(4)请写出下列反应的化学方程式:
①A→H_________________________________________________________;
②B→D(第①步)______________________ _________________________。
查看答案和解析>>
科目:高中化学 来源:2013-2014浙江省高一下学期期末考试化学试卷(解析版) 题型:选择题
两种微粒含有相同的质子数和电子数,这两种微粒可能是
①两种不同的原子;②两种不同元素的原子;③一种原子和一种分子;④一种原子和一种离子;⑤两种不同分子;⑥一种分子和一种离子;⑦两种不同阳离子;⑧两种不同阴离子;⑨一种阴离子和一种阳离子
A.①③⑤⑥⑦⑧ B.①③⑤⑦⑧
C.①③④⑤⑦ D.全部都是
查看答案和解析>>
科目:高中化学 来源:2013-2014浙江省宁波市高二下学期期末考试化学试卷(解析版) 题型:选择题
将一定量的氯气通入30 mL浓度为10.00 mol/L的氢氧化钠浓溶液中,加热少许时间后溶液中形成NaCl、NaClO、NaClO3共存体系。下列判断正确的是 ( )
A.与NaOH反应的氯气一定为0.3 mol
B.n(Na+)∶n(Cl-)可能为7∶3
C.若反应中转移的电子为n mol,则0.15<n<0.25
D.n(NaCl)∶n(NaClO)∶n(NaClO3)可能为11∶2∶1
查看答案和解析>>
科目:高中化学 来源:2013-2014浙江省宁波市高二下学期期末考试化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值。下列说法一定正确的是 ( )
A.常温下,1 L 0.1 mol/L的NH4NO3溶液中氧原子数为0.3NA
B.1 mol的羟基与1 mol的氢氧根离子所含电子数均为10NA
C.常温、常压下,4.6 g NO2和N2O4混合气体中含有的O原子数目为0.2NA
D.Fe与水蒸气在高温条件下反应,有1 mol Fe参与反应,则转移电子的数目为3NA
查看答案和解析>>
科目:高中化学 来源:2013-2014浙江省宁波市高一下学期期末考试化学试卷(解析版) 题型:选择题
用惰性电极电解下列足量的溶液,一段时间后,再加入一定量的另一物质(括号内)后,溶液能与原来溶液浓度一样的是 ( )
A.CuCl2(CuCl2溶液) B.AgNO3(Ag2O) C.NaCl(HCl溶液) D.CuSO4(Cu(OH)2)
查看答案和解析>>
科目:高中化学 来源:2013-2014浙江省宁波市高一下学期期末考试化学试卷(解析版) 题型:选择题
下列说法错误的是( )
A.一般的水是由10个以上的水分子聚结组成一个水分子团,叫大分子团水,科学家能把大分子团水变成5-8个水分子组成的小分子团水,一次饮用125 mL可维持人体6小时正常需水量,这个转变过程改变了水分子间的结构和物理性质
B.离子化合物中可能有共价键
C.科学家在青藏高原深处发现了天然的氮化硼(BN,具有高熔点、高密度、高硬度等特性),它可能是原子晶体
D.用“撕裂”方法可从石墨材料中剥离出的单层碳原子面材料(石墨烯),用这种方法从C60、金刚石等碳原子中获得“只有一层碳原子厚的碳薄片”也将成为研究方向
查看答案和解析>>
科目:高中化学 来源:2013-2014浙江省台州市路桥区高考理综化学模拟试卷二试卷(解析版) 题型:选择题
下列说法正确的是 ( )
A.用酸性高锰酸钾即可鉴别苯酚溶液,2,4-己二烯和甲苯
B. 按系统命名法化合物 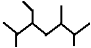 的名称为:2,5,6-三甲基-3-乙基庚烷
的名称为:2,5,6-三甲基-3-乙基庚烷
C. 新型解热镇痛抗炎药贝诺酯 在酸性条件下完全水解可以得到3种有机物
在酸性条件下完全水解可以得到3种有机物
D.β—月桂烯的结构如图 ,一分子该物质与两分子溴发生加成反应的产物(只考虑位置异构)理论上最多有3种
,一分子该物质与两分子溴发生加成反应的产物(只考虑位置异构)理论上最多有3种
查看答案和解析>>
科目:高中化学 来源:2013-2014浙江省下学期第二次统练高一化学试卷(解析版) 题型:实验题
某同学为探究铜跟浓硫酸的反应情况,用下图所示装置进行了有关实验
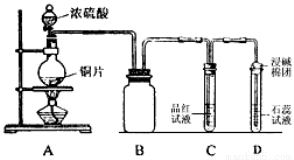
(1)B是用来收集实验中生成的气体的装置,但未将导管画全,请在答题卷上把导管补充
完整 。
(2)请写出铜跟浓硫酸反应的化学方程式 。
(3)实验中D中的现象 。
(4)实验中,该同学取6.4g铜片和12mL 18mol·L-1H2SO4溶液放在圆底烧瓶中共热,直到反应停止,最后发现烧瓶中还有铜片剩余;该同学根据所学的化学知识判断还会有一定量H2SO4的剩余,下列药品中能够用来验证反应停止后的烧瓶中确有剩余的H2SO4的是 填字母编号)。
a.BaCl2溶液 b.Ba(NO3)2溶液 c.银粉 d.Na2CO3粉末
(5)若将16g铜与50mLH2SO4物质的量浓度为一定值的浓硫酸反应,铜完全溶解。请回答:
①反应中产生的气体在标准状况下的体积为 L。
②该反应中被还原的H2SO4的物质的量为 mol。
③待产生的气体全部释放后,向溶液中滴加VmL a mol·L-1NaOH溶液,恰好使溶液中
的Cu2+全部转化为沉淀,则原浓硫酸中H2SO4的物质的量浓度= mol·L-1。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com