
【题目】某气态有机物X含C、H、O三种元素,已知下列条件,现欲确定X的分子式,所需最少条件是 ( )
①X中含碳质量分数 ②X中含氢质量分数③X在标准状况下的体积 ④X对H2的相对密度⑤X的质量
A.①②B.①②④
C.①②⑤D.③④⑤
科目:高中化学 来源: 题型:
【题目】图中甲池的总反应式为2CH3OH+3O2+4KOH=2K2CO3+6H2O,下列说法正确的是 ( )
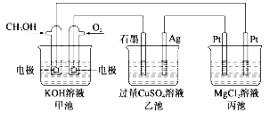
A.甲池电能转化为化学能,乙、丙池化学能转化为电能
B.甲池中通入CH3OH的电极反应式为: CH3OH-6e-+2H2O= CO+8H+
C.甲中消耗280 mL(标准状况下)O2时,丙池理论上最多产生1.45 g固体
D. 反应一段时间后,向乙池中加入一定量Cu(OH)2固体能使CuSO4溶液恢复到原浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用KClO3分解(MnO2做催化剂)制取氧气,实验后回收剩余固体中的MnO2,正确的操作步骤是
A. 溶解、过滤、蒸发 B. 溶解、过滤、洗涤、干燥
C. 溶解、过滤、结晶 D. 溶解、结晶、干燥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】玻璃、水泥和陶瓷均为硅酸盐制品,下列有关说法正确的是( )
A.玻璃是人类最早使用的硅酸盐制品
B.制造水泥的主要原料为纯碱、石灰石和石英
C.硅酸盐制品的性质稳定、熔点较高
D.制造水泥的过程中只发生了物理变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组对过量炭粉与氧化铁反应的气体产物成分进行研究。
(1)提出假设 ①该反应的气体产物是CO2。 ②该反应的气体产物是CO。③该反应的气体产物是______________。
(2)设计方案 如图所示,将一定量的氧化铁在隔绝空气的条件下与过量炭粉完全反应,测定参加反应的碳元素与氧元素的质量比。
(3)查阅资料
氮气不与碳、氧化铁发生反应。实验室可以用氯化铵饱和溶液和亚硝酸钠(NaNO2)饱和溶液混合加热反应制得氮气。请写出该反应的离子方程式:_________________________________。
(4)实验步骤

①按上图连接装置,并检查装置的气密性,称取3.20g氧化铁、2.00g碳粉混均匀,放入48.48g的硬质玻璃管中;
②加热前,先通一段时间纯净干燥的氮气;
③停止通入N2后,夹紧弹簧夹,加热一段时间,澄清石灰水(足量)变浑浊;
④待反应结束,再缓缓通入一段时间的氮气。冷却至室温,称得硬质玻璃管和固体总质量为52.24g;
⑤过滤出石灰水中的沉淀,洗涤、烘干后称得质量为2.00g。
步骤②、④中都分别通入N2,其作用分别为_________________________________。
(5)数据处理
试根据实验数据分析,写出该实验中氧化铁与碳发生反应的化学方程式:__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中![]() H>0,
H>0,![]() S>0的是
S>0的是
A. 2Mg(s) + CO2(g)→ 2MgO(s) + C(s)
B. 低温下能自发进行的反应:NH3(g)+HCl(g) →NH4Cl(s)
C. 高温下能自发进行的反应:SiO2(s) +2C(s) →Si(s)+2CO(g)
D. 任何温度下均能自发进行的反应:2H2O2(l) → 2H2O(l) + O2(g)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,当关闭阀门K时,向甲中充入1.5 mol A、3.5 mol B,向乙中充入3 mol A、7 mol B,起始时,甲、乙体积均为V L。在相同温度和有催化剂存在的条件下,两容器中各自发生下列反应:3A(g)+ 2B(g)![]() C(g)
C(g)![]() +2D(g);ΔH<0达到平衡(Ⅰ)时,V(乙)=0.86V L。请回答:
+2D(g);ΔH<0达到平衡(Ⅰ)时,V(乙)=0.86V L。请回答:
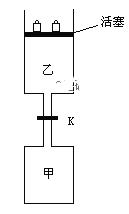
(1)乙中B的转化率为______________;
(2)甲中D和乙中C的物质的量比较:__________(填“相等”、“前者大”、“后者大”);
(3)打开K,过一段时间重新达平衡(Ⅱ)时,乙的体积为________(用含V的代数式表示,连通管中气体体积忽略不计)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某温度时,将nmol/L氨水滴入10mL1.0mol/L盐酸中,溶液pH和温度随加入氨水体积变化曲线如图所示,下列有关说法正确的是( )

A. a点Kw=1.0×10-14
B. 水的电离程度:b>c>a>d
C. b点:c(NH4+)>c(Cl-)>c(H+)>c(OH-)
D. 25℃时,NH4Cl水解常数为(n-1)×10-7(用n表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】pH=1的某溶液X中仅含有NH4+、Al3+、Ba2+、Fe2+、Fe3+、CO32﹣、SO32﹣、SO42﹣、Cl﹣、NO3﹣中的一种或几种(忽略水的电离及离子的水解),取该溶液进行连续实验,实验过程如图:下列有关推断不正确的是( )
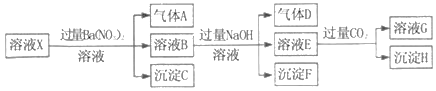
A. 溶液X中一定含有H+、Al3+、NH4+、Fe2+、SO42﹣
B. 根据上述连续实验不能确定溶液X中是否含有Fe3+、Cl﹣
C. 沉淀H为Al(OH)3、BaCO3的混合物
D. 若溶液X为100mL,产生的气体A为44.8mL(标准状况),则X中c(Fe2+)=0.06molL﹣1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com