
【题目】一定温度下,在三个体积均为![]() 恒容密闭容器中发生反应:
恒容密闭容器中发生反应:
![]()
下列说法正确的是![]()
窗口编号 | 温度 | 起始物质的量 | 平衡物质的量 | |
|
|
| ||
1 | 380 |
|
|
|
2 | 380 |
| ||
3 | 230 |
|
|
|
A.该反应的正反应为放热反应
B.达到平衡时,容器1中的![]() 体积分数比容器2中的小
体积分数比容器2中的小
C.容器1中反应达到平衡所需的时间比容器3中的长
D.若起始时向容器Ⅲ中充入![]()
![]()
![]() 、
、![]()
![]()
![]() 和
和![]()
![]() ,则反应向逆反应方向进行
,则反应向逆反应方向进行
【答案】D
【解析】
A. 容器Ⅰ中平衡时c(苯乙烯)=0.6mol/L, (H2)=0.06mol/L,c(乙苯)=(0.1mol0.06mol)÷1L=0.04mol/L,容器Ⅰ中化学平衡常数K1=0.06×0.6÷0.04=0.9,容器Ⅲ中平衡时c(苯乙烯)=c(H2)=0.05mol/L,c(乙苯)=0.05mol/L,化学平衡常数K2=0.05×0.05÷0.05=0.05<0.9,所以降低温度,化学平衡常数降低,则正反应是吸热反应,故A错误;
B. 恒容条件下,容器Ⅱ相当于在容器Ⅰ的基础上加压,但由于该反应是反应前后气体体积不变的反应,因此平衡不移动,所以容器Ⅰ中的H2体积分数和容器Ⅱ中的相等,故B错误;
C. 容器Ⅰ中的温度比容器III的温度高,温度越高反应速率越快,达到平衡所需时间越短,故C错误;
D. 若起始时向容器Ⅲ中充入0.10mol![]() (g)、0.10mol
(g)、0.10mol![]() (g)和0.10molH2,浓度商=0.1×0.1÷0.1=0.1>0.05,平衡向逆反应方向移动,故D正确;
(g)和0.10molH2,浓度商=0.1×0.1÷0.1=0.1>0.05,平衡向逆反应方向移动,故D正确;
故选:D。


 课堂练加测系列答案
课堂练加测系列答案 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案科目:高中化学 来源: 题型:
【题目】某烷烃的结构简式是CH3CH2CH(CH2CH3)CH3,它的正确命名是
A. 2-乙基丁烷 B. 3-乙基丁烷
C. 3-甲基戊烷 D. 2,2-二甲基丁烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫及其化合物有许多用途,相关物质的物理常数如表所示:
H2S | S8 | FeS2 | SO2 | SO3 | H2SO4 | |
熔点/℃ | -85.5 | 115.2 | >600(分解) | -75.5 | 16.8 | 10.3 |
沸点/℃ | -60.3 | 444.6 | -10.0 | 45.0 | 337.0 |
回答下列问题:
(1)基态S原子电子占据最高能级的电子云轮廓图为___形。
(2)根据价层电子对互斥理论,H2S、SO2、SO3的气态分子中,中心原子价层电子对数不同其他分子的是__。
(3)图(a)为S8的结构,其硫原子的杂化轨道类型为___。
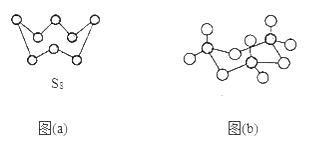
(4)气态三氧化硫以单分子形式存在,其分子的立体构型为___形;固体三氧化硫中存在如图(b)所示的三聚分子,该分子中S原子的杂化轨道类型为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是
A. 14g乙烯中所含氢原子数为2NA
B. 6g14C原子中所含中子数为4NA
C. 标准状况下2.24LHC1气体中所含H+数为0.1NA
D. 0.1mol氯气溶于水制成饱和氯水,转移电子数目为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由一氯乙烷合成乙二醇的线路如下:
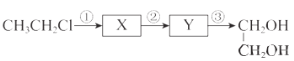
(1)反应①发生消去反应,反应试剂和条件为________________。
(2)反应②选用的无机试剂为_________________。
(3)反应③的化学方程式是___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据量子力学计算,氮化碳结构有五种,其中一种β-氮化碳硬度超过金刚石晶体,成为首屈一指的超硬新材料,已知该氮化碳的二维晶体结构如图所示。下列有关氮化碳的说法不正确的是

A. 该晶体中的碳、氮原子核外都满足8电子稳定结构
B. 氮化碳中碳显+4价,氮显-3价
C. 每个碳原子与四个氮原子相连,每个氮原子和三个碳原子相连
D. 氮化碳的分子式为C3N4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Y、Z、W、R、M五种元素,位于元素周期表的前四周期,它们的核电荷数依次增大,有如下信息:
元素 | 相关信息 |
Y | 原子核外有6个不同运动状态的电子 |
Z | 非金属元素,基态原子的s轨道的电子总数与p轨道的电子总数相同 |
W | 主族元素,与Z原子的价电子数相同 |
R | 价层电子排布式为3d64s2 |
M | ⅠB族,其单质常用作导线 |
请回答下列问题(Y、Z、W、R、M用所对应的元素符号表示):
(1)Z、W元素相比,第一电离能较大的是_____________________,M2+的核外电子排布式为________________________。
(2)写出两个与YZ2互为等电子体的化学式_________________ 。
(3)WZ2分子中W原子价层电子对数是_____________对,WZ2的VSEPR 模型名称为_______________,WZ3气态为单分子,该分子中W原子的杂化轨道类型为__________________;WZ3的三聚体环状结构如图所示,该结构中W原子的杂化轨道类型为__________;该结构中W-Z键长有两类,一类键长约140pm,另一类键长约为160pm,较短的键为___________(填图中字母) ,该分子中含有______个σ键。
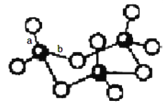
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA代表阿伏加德罗常数的值。下列说法正确的是
A. 常温常压下,124 g P4中所含P—P键数目为4NA
B. 100 mL 1mol·L1FeCl3溶液中所含Fe3+的数目为0.1NA
C. 标准状况下,11.2 L甲烷和乙烯混合物中含氢原子数目为2NA
D. 密闭容器中,2 mol SO2和1 mol O2催化反应后分子总数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以高硫铝土矿(主要成分为Al2O3、Fe2O3,还含有少量FeS2)为原料,生产氧化铝并获得Fe3O4的部分工艺流程如下,下列叙述不正确的是
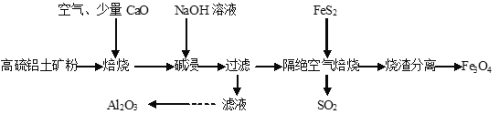
A.加入CaO可以减少SO2的排放同时生成建筑材料CaSO4
B.向滤液中通入过量HCl气体、过滤、洗涤、灼烧沉淀可制得Al2O3
C.隔绝空气焙烧时理论上反应消耗的n(FeS2):n(Fe2O3)=1:5
D.烧渣分离可用磁选法
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com