
①6NH4Al(SO4)2·12H2O![]() 3Al2O3+6SO3↑+6SO2+2NH3↑+2N2↑+21H2O?
3Al2O3+6SO3↑+6SO2+2NH3↑+2N2↑+21H2O?
②6NH4Al(SO4)2·12H2O![]() 3Al2O3+9SO3↑+3SO2↑+4NH3↑+N2↑+18H2O等等。?
3Al2O3+9SO3↑+3SO2↑+4NH3↑+N2↑+18H2O等等。?
(1)铝铵明矾受热分解反应中,氧化产物是__________,还原产物是__________,它们的物质的量之比为__________。?
(2)把上述反应中的Al2O3加入适量氧化铬在氢氧焰上强热熔融后,使其结晶可以制成人造红宝石,可用于作激光器材和装饰品。所得人造红宝石是哪种Al2O3晶体?怎样用简便方法说明它确实是该种Al2O3的晶体? ??????
解析:(1)反应中,N元素化合价由-3→0,氧化产物是N2;S元素化合价由+6→+4,还原产物是SO2。①反应中:?n(N2)∶n(SO2)=1∶3;②反应中:n(N2)∶n(SO2)?=1∶3,可见氧化产物与还原产物的物质的量之比为1∶3。
(2)由题意,α-Al2O3可以用γ-Al2O3高温煅烧制得,而红宝石也是由Al2O3和Cr2O3高温熔融制得的,所以可以确认红宝石的主要成分是α-Al2O3。
由题意,γ-Al2O3不耐酸,α-Al2O3对酸有极强稳定性。红宝石是不是α-Al2O3可放在强酸溶液中鉴定。
答案:(1)N2 SO2 1∶3
(2)?α-Al2O3。取少量样品放入稀盐酸中,若样品溶解,则为γ-Al2O3;若样品不溶解,则为?α-Al2O3。


 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源: 题型:
(1)判断赛伦属于 晶体类型,并且有 等特性(至少写出三种)。
(2)化学通式里y值为 (用含x的表达式或某一具体数值表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
在氮化硅中添加氧化铝,用氧原子取代一部分氮,用铝原子取代一部分硅,通过常压烧结即成为新一代无机非金属材料,叫氧氮化硅铝,即赛伦(Sialon),化学通式为Si6-xAlxOxNy(x:2~4)。
(1)判断赛伦属于 晶体类型,并且有 等特性(至少写出三种)。
(2)化学通式里y值为 (用含x的表达式或某一具体数值表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
(12分)原子序数由小到大排列的X、Y、Z三种短周期元素,已知三种元素的原子序数之和等于16, 单质X2 、Y2 、Z2之间有如下转化关系(反应条件已略)。已知:甲、乙分子中均含有10个电子;丙分子中含有15个电子。请回答:
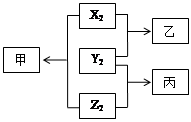
(1)Y2的电子式是___ ______;该分子中有 个σ键, 个π键。
(2)甲属于(填“极性”或“非极性”) 分子;晶体中甲分子的配位数为 。
(3)乙分子的VSEPR模型名称为 ,分子的立体构型名称为 。
(4)写出乙与Z2反应生成丙的化学方程式 。
(5)工业上用氧化铝、碳和乙在1400℃条件下反应,制取由元素Y和Al组成的化合物丁,同时还有CO和X2生成。已知反应中消耗1mol乙,可生成1.5molCO和1.5molX2。写出反应的化学方程式: ,氧化剂为 。
查看答案和解析>>
科目:高中化学 来源:2010—2011学年湖北省武穴中学高二3月月考化学试卷 题型:填空题
(12分)原子序数由小到大排列的X、Y、Z三种短周期元素,已知三种元素的原子序数之和等于16,单质X2 、Y2 、Z2之间有如下转化关系(反应条件已略)。已知:甲、乙分子中均含有10个电子;丙分子中含有15个电子。请回答: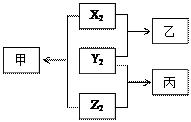
(1)Y2的电子式是___ ______;该分子中有 个σ键, 个π键。
(2)甲属于(填“极性”或“非极性”) 分子;晶体中甲分子的配位数为  。
。
(3)乙分子的VSEPR模型名称为 ,分子的立体构型名称为 。
(4)写出乙与Z2反应生成丙的化学方程式 。
(5)工业上用氧化铝、碳和乙在1400℃条件下反应,制取由元素Y和Al组成的化合物丁,同时还有CO和X2生成。已知反应中消耗1mol乙,可生成1.5molCO和1.5molX2。写出反应的化学方程式: ,氧化剂为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com