
| A. | 钠 | B. | 碳 | C. | 氮 | D. | 硫 |
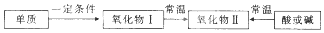
分析 根据转化图氧化物在常温下能转化为另一种氧化物的是一氧化氮到二氧化氮的转化,其他氧化物如一氧化碳、二氧化硫转化为二氧化碳、三氧化硫都需要条件,据此来回答.
解答 解:A、金属钠对应的碱即为氢氧化钠,在常温下不会转化为过氧化钠,故A错误;
B、碳单质的氧化物一氧化碳转化为二氧化碳需要点燃,常温下不能进行,故B错误;
C、氮气和氧气在闪电条件下转化为一氧化氮,一氧化氮常温下迅速变为二氧化氮,二氧化氮可以用浓硝酸来制取,故C正确;
D、硫单质燃烧生成的二氧化硫在高温高压催化剂作用下才转化为三氧化硫,常温下不能进行,故D错误.
故选C.
点评 本题考查学生元素以及化合物性质知识,注意变价元素所在的物质的性质是解题关键,难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该混盐能使高锰酸钾酸性溶液褪色 | |
| B. | 该混盐溶液加入BaCl2可以生成沉淀 | |
| C. | 该混盐与H2SO4反应有气体生成 | |
| D. | 该混盐在酸性条件下可生成S,每产生1molS转移1.5NA个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| T/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com