
用50 mL 0.55 mol/L盐酸与50 mL 0.50 mol/L NaOH溶液进行中和热测定的实验,测量结果偏高的原因可能是( )
| A.实验装置保温、隔热效果差 |
| B.用温度计测定NaOH溶液起始温度后直接测定盐酸的温度 |
| C.量取NaOH溶液的体积时仰视读数 |
| D.分多次把NaOH溶液倒入盛有盐酸的小烧杯中 |
 智能训练练测考系列答案
智能训练练测考系列答案 计算高手系列答案
计算高手系列答案科目:高中化学 来源: 题型:038
对牛奶中的蛋白质进行实验:取30.0 mL牛奶,用盖尔达法分解蛋白质,把其中所含的氮元素完全转变为氨,再用50 mL 0.5 mol·![]() 的硫酸溶液充分吸收,剩余的硫酸用1 mol·
的硫酸溶液充分吸收,剩余的硫酸用1 mol·![]() 的氢氧化钠溶液中和,消耗NaOH溶液38.00
mL.
的氢氧化钠溶液中和,消耗NaOH溶液38.00
mL.
求:(1)已知蛋白质中含氮质量分数为16%,求该牛奶中蛋白质的质量分数.(该牛奶的密度是1.03 g·![]() )
)
(2)在250.0 mL牛奶中含蛋白质的质量.
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:038
求:(1)已知蛋白质中含氮质量分数为16%,求该牛奶中蛋白质的质量分数.(该牛奶的密度是1.03 g·![]() )
)
(2)在250.0 mL牛奶中含蛋白质的质量.
查看答案和解析>>
科目:高中化学 来源: 题型:
A.用10 mL量筒准确量取稀硫酸溶液8.0 mL
B.用干燥的pH试纸测定氯水的pH
C.用碱式滴定管量取KMnO4溶液19.60 mL
D.使用容量瓶配制溶液时,俯视液面定容后所得溶液的浓度偏大
E.将饱和FeCl3溶液滴入蒸馏水中即得Fe(OH)3胶体
F.圆底烧瓶、锥形瓶、蒸发皿加热时都应垫在石棉网上
(2)用50 mL 0.5 mol·L-1的盐酸与50 mL 0.55 mol·L-1的NaOH溶液进行中和热的测定实验,请回答下列问题:
①在实验中使用的仪器除大烧杯、小烧杯、环形玻璃搅拌棒、泡沫塑料或纸条、泡沫塑料板或硬纸板(中心有两个小孔)外,还必须要用到的仪器有___________________________。
②要想提高中和热测定的准确性,可采用的措施除以下列出的三种以外,请你再写出三种:
a.如果按教材中的方法做,一定要使小烧杯杯口与大烧杯杯口相平。
b.盐酸和NaOH溶液浓度的配制要准确,且NaOH溶液的浓度须稍大于盐酸的浓度。
c.实验操作时动作要快,注意不要将溶液洒到外面。
d.__________________________________________________________。
e.__________________________________________________________。
f.__________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
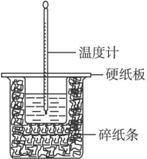
A.实验过程中没有热量损失
B.图中实验装置缺少环形玻璃搅拌棒
C.烧杯间填满碎纸条的作用是固定小烧杯
D.若改用60 mL 0.50 mol·L-1盐酸跟50 mL 0.55 mol·L-1的NaOH溶液进行反应,从理论上说所求中和热不相等
查看答案和解析>>
科目:高中化学 来源: 题型:
三鹿奶粉事件震惊全国,导致了中国奶制品行业危机,其起因是掺假者为了提高奶制品中蛋白质含量而加入了化工原料三聚氰胺(C3N6H6),严重损害了人们的身体健康。测定牛奶中蛋白质含量常用盖达尔法:![]() ,如图所示为某一牛
,如图所示为某一牛
奶的营养成分表,现取30 mL牛奶用盖达尔法分解蛋白质,把氮全部转化为氨,用50 mL 0.5 mol/L的H2SO4吸收,剩余的酸用1 mol/L NaOH溶液中和,需38 mL。
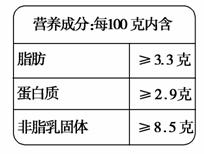
(1)计算30 mL牛奶中共含有多少克氮?
(2)试判断此牛奶中蛋白质含量是否合格(已知牛奶密度为1.3 g·mL-1,蛋白质中含氮的质量分数为16%)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com