

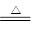 CaCO3+CO↑ (2分)
CaCO3+CO↑ (2分)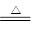 CaC2O4+H2O↑
CaC2O4+H2O↑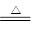 CaCO3+CO↑
CaCO3+CO↑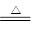 CaCO3+CO↑
CaCO3+CO↑ CaO+CO2↑。由此得出C的化学式为CaO,其分子量即为56.
CaO+CO2↑。由此得出C的化学式为CaO,其分子量即为56.

 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案科目:高中化学 来源:不详 题型:单选题
| A.9g水所含电子数为 5NA |
| B.常温常压下1 mol NO2气体与水在无氧条件下反应生成NA个NO3-离子 |
| C.标准状况下,11.2L三氧化硫溶于水,可生成0.5NA个硫酸分子 |
| D.62 g Na2O溶于水后所得溶液中含有Na+ 离子数为NA |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.使用容量瓶配制溶液时, 俯视液面定容后所得溶液的浓度 |
| B.没有用蒸馏水洗烧杯2-3次,并将洗液移入容量瓶中 |
| C.容量瓶用蒸馏水洗净,没有烘干 |
| D.定容时,滴加蒸馏水时液面略高于刻度线,再吸出少量水使液面凹面与刻度线相切 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.反应①中O2是氧化产物,反应②中水是氧化剂 |
| B.该热化学循环制氢过程简单、无污染,物料可循环使用,安全易分离 |
| C.若MnFe2O(4-x)(s)中x=0.8,则MnFe2O(4-x)(s)中Fe2+占全部铁元素的百分率为60% |
| D.若xH2(g)+x/2O2 (g)=xH2O(g);△H3,则△H3=-(△H1+△H2) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.1.14×10—3 mol?L—1 | B.0.2 mg?mL—1 |
| C.1.42×10—3 mol?L—1 | D.0.2 mol?L—1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在H2O2+Cl2=2HCl+O2反应中,每生成32g氧气,则转移2NA个电子 |
| B.10mL质量分数为98%的H2SO4,用水稀释至100mL,H2SO4的质量分数为9.8% |
| C.一定温度下,1molFeCl3水解生成NA个Fe(OH)3胶体颗粒 |
| D.在标准状况下,2.24L苯中所含分子数约为NA |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.16 g甲烷分子中含有共价键的数目为2NA |
| B.常温常压下,30克葡萄糖含有的氧原子数为NA |
| C.0.1mol·L-1的AlCl3溶液中含有的氯离子数为0.3NA |
| D.25℃时, 1 L 0.1mol/L的CH3COOH溶液中的H+数为0.1 NA |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.SO2的摩尔质量是64g |
| B.18g H2O在标准状况下的体积是22.4L |
| C.在标准状况下,20mL NH3与60mL O2所含的分子数比为1:3。 |
| D.将40g NaOH溶于1L水中,所得溶液的物质的量浓度为1mol/L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com