
| A. | N、O、S | B. | Cl、S、O | C. | Si、P、N | D. | S、Cl、F |
分析 X、Y、Z是周期表中相邻的三种元素,其中X、Y在同一周期,Y、Z在同一主族,且这三种元素原子最外层电子数之和为19,质子数总和为41,根据三种元素的最外层电子数之和确定三种元素的主族序数,再结合其质子数总数确定元素,由此分析解答.
解答 解:X、Y、Z是周期表中相邻的三种元素,其中X、Y在同一周期,Y、Z在同一主族,且这三种元素原子最外层电子数之和为19,质子数总和为41,设Z、Y的最外层电子数是a,X的最外层电子数是a+1,a+a+a+a+1=19,a=6,所以Y和Z属于第VIA族元素、X属于第VIⅠA族元素,质子数总和为41,设Z的质子数是b、Y的质子数是b+8,X的质子数是b+9,b+b+8+b+9=38,所以b=8,所以Z是O元素、Y是S元素、X是Cl元素,
故选B.
点评 本题考查了原子结构和元素性质,明确原子结构、元素周期表结构是解本题关键,再根据最外层电子数、质子数来确定元素,题目难度不大.


科目:高中化学 来源: 题型:填空题
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向2mL 2%CuSO4溶液中加入0.5mL 1%的NaOH溶液,振荡后滴加M溶液,加热 | 未出现砖红色沉淀 | M中不含醛基 |
| B | 在CuSO4溶液中介入KI溶液,再加入苯,振荡后静置 | 有白色沉淀生成,苯层呈紫红色 | 白色沉淀可能为CuI |
| C | 向有机试剂N中加入2mL5%的NaOH溶液,加热,冷却后取上层溶液滴加几滴AgNO3溶液 | 出现褐色沉淀 | N不是卤代烃 |
| D | 将Fe(NO3)2样品溶于稀H2SO4后,滴加KSCN溶液 | 溶液变为血红色 | Fe(NO3)2已氧化变质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
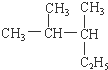 2,3-二甲基戊烷
2,3-二甲基戊烷
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 若a为浓硫酸,b为Na2SO3固体,c中盛紫色石蕊溶液,则c中溶液变红 | |
| B. | 若a为醋酸溶液,b为贝壳,c中盛过量澄清石灰水,则c中溶液变浑浊 | |
| C. | 若a为浓盐酸,b为MnO2,c中盛品红溶液,则c中溶液褪色 | |
| D. | 若a为浓氨水,b为生石灰,c中盛AlCl3溶液,则c中产生白色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验序号 | 1 | 2 | 3 | 4 |
| 消耗NaOH溶 液的体积(mL) | 20.05 | 20.00 | 18.50 | 19.95 |
| 醋酸浓度 (mol/L) | 0.0010 | 0.0100 | 0.0200 | 0.1000 | 0.2000 |
| pH | 3.88 | 3.38 | 3.23 | 2.88 | 2.73 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 熔点:金刚石>食盐>干冰 | B. | 热稳定性:HCl>H2S>PH3 | ||
| C. | 沸点:HF>HBr>HCl | D. | 离子半径:Na+<Mg2+<Al3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 )广泛用于集成电路的制备和微细图形的加工.下面是有机物X的一种合成路线:
)广泛用于集成电路的制备和微细图形的加工.下面是有机物X的一种合成路线: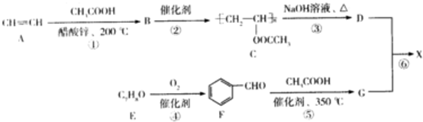

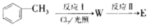
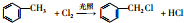 ,反应Ⅱ的试剂为氢氧化钠水溶液、加热.
,反应Ⅱ的试剂为氢氧化钠水溶液、加热.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

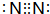 ,E的化学式为NO.
,E的化学式为NO.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com