
【题目】反应条件是影响有机化学反应的重要因素。下列各组物质的反应产物与反应条件无关的是( )
A. 甲苯与溴
B. 丙烯与溴的CCl4溶液
C. 溴乙烷与氢氧化钠溶液
D. 乙醇与氧气
科目:高中化学 来源: 题型:
【题目】有兴趣研究小组用工业废渣(主要成分为Cu2S和Fe2O3)制取氯化亚铜并同时生成电路板蚀刻液。资料显示:氯化亚铜(化学式为CuCl)常用作有机合成工业中的催化剂,通常是一种白色粉末,微溶于水、不溶于乙醇,在潮湿空气中易水解氧化成绿色;见光则分解。
他们设计流程如下:
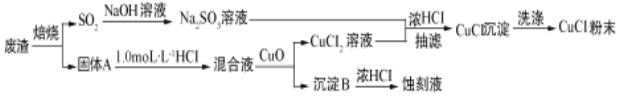
据此流程和以上信息回答下列问题:
(1)验证焙烧气体产物是SO2的方法______________________________________;溶解固体A对应的化学方程式为_____________________________________。
(2)SO2吸收用NaOH溶液,为得到纯净的Na2SO3溶液,其操作应为_____________________________________________________________________。
(3)在Na2SO3的水溶液中逐滴加入CuCl2溶液,再加入少量浓盐酸混匀,倾出清液,抽滤即得CuCl沉淀.写出该反应的离子方程式______。
(4)CuCl沉淀的洗涤需要经过酸洗、水洗和醇洗,水洗操作为____________________;醇洗不能省略,原因是______。
(5)得到CuCl沉淀要迅速真空干燥、冷却,密封包装。这样操作的目的是_______________________________________________________。
(6)氯化亚铜在热水中迅速与水反应生成砖红色固体,写出该反应的化学方程式_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1体积的某烃蒸气完全燃烧生成的CO2比水蒸气少1体积(同温同压下),0.1 mol该烃完全燃烧的产物被碱石灰吸收,碱石灰增重39 g,则该烃的分子式为( )
A. C6H14 B. C5H12
C. C7H16 D. C6H6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列叙述正确的是
A. NA个H2分子占有的体积一定为22.4 L
B. 标准状况下,22 g CO2与11.2 LH2O含有相同的原子数
C. 标准状况下,16g O2与O3的混合气体中含有的原子总数为NA
D. 1 mol/L的蔗糖水溶液中含蔗糖分子的数目为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是

A. 由图甲表示的反应速率随温度变化的关系可知该反应的ΔH>0
B. 图乙表示pH相同的盐酸与氢氟酸分别加水稀释PH的变化,其中曲线a对应的是氢氟酸
C. 图丙表示该反应为放热反应,且催化剂能改变反应的焓变
D. 图丁表示向Na2CO3溶液中逐滴滴加稀盐酸,生成CO2与所加盐酸物质的量的关系
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据要求填空:
(1)FeSO4可转化为FeCO3,FeCO3在空气中加热可制得铁系氧化物材料
已知25℃,101kPa时:4Fe(s)+3O2(g)=2Fe2O3(s)ΔH=-1648kJ/mol
C(s)+O2(g)=CO2(g) ΔH=-393kJ/mol
2Fe(s)+2C(s)+3O2(g)=2FeCO3(s) ΔH=-1480kJ/mol
FeCO3在空气中加热反应生成Fe2O3的热化学方程式为_______.
(2)某温度时水的离子积Kw=1.0×10-13,则该温度时纯水的pH____7(填“>”、“<”或“=”)。该温度下,pH=2的CH3COOH溶液中,c(OH-)=_________。
(3)向2份0.1mol/LCH3COONa溶液中分别加人少量NH4NO3、Na2SO3固体(忽略体积变化),则CH3COO-浓度的变化依次为_____、______ (填“减小”“增大”或“不变”)。
(4)同浓度的NaA和NaB两种溶液pH前者大于后者,比较两份溶液中所含阴阳离子总浓度大小, NaA_______NaB (填">”、“<”或“=")。
(5)25℃时,某溶液中Fe3+的浓度为0.010mol/L,使Fe3+沉淀完全的pH为____。(Ksp[Fe(OH)3]=4×10-38,1g2=0.3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环扁桃酯是用于治疗心脑血管疾病的重要化合物。它的一种合成路线如下
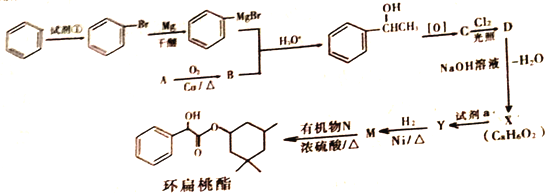
已知: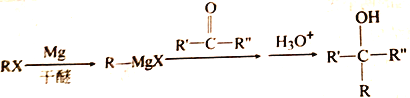 (R、R'、R〞代表烃基或氢)
(R、R'、R〞代表烃基或氢)
(1)试剂①为__________________________;
(2)写出A生成B的反应方程式______________________________;
(3)X的结构简式是______________,X→Y的反应类型是_______________________;
(4)M与N生成环扁桃酯的化学方程式是_______________________;
(5)有机物Z与Y 互为同分异构体,满足下列条件的有机物Z的结构有___________种,写出任意一种核磁共振氢谱中有4个峰,且面积之比为2 :2 :1:1的同分异构体的结构简式为_________________;
①芳香族化合物 ②能发生银镜反应,且1mol与足量的银氨溶液反应生成4molAg
(6)以CH2=CHCH3、CH3CHO为有机原料,结合题目所给信息,选用必要的无机试剂合成CH=CHCH=CHCH3,合成路线为:CH2=CHCH3![]() E
E![]() CH2=CHCH2MgBr
CH2=CHCH2MgBr![]() F
F![]() CH2=CHCH=CHCH3
CH2=CHCH=CHCH3
请依次写出反应①到④反应条件和试剂,写出E、F的结构简式________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温、恒容下,有下列气体反应分别从两条途径进行:

下列叙述正确的是( )
A. Ⅰ、Ⅱ两条途径最终达到平衡时,体系内混合气体的百分组成相同
B. Ⅰ、Ⅱ两条途径最终达到平衡时,体系内混合气体的浓度相同
C. 达到平衡时,Ⅰ途径所用的时间与Ⅱ途径所用的时间相同
D. 达到平衡时,Ⅰ途径混合气体密度等于Ⅱ途径混合气体的密度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】掌握仪器的名称、组装及使用方法是中学化学实验的基础,如图为两套实验装置。


(1)写出下列仪器的名称:①_______;④ ______
(2)仪器①~④中,使用时必须检查是否漏水的有___________;图I实验过程中使用冷凝管时应从_______处进水。(均填序号)
(3)若利用装置I分离四氯化碳和酒精的混合物,还缺少的仪器有________;将仪器补充完整后进行的实验操作的名称为:___________。现需配制500 ml 0.2 mol/L NaCl溶液,装置II是某同学转移溶液的示意图,图中的错误是 _____________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com