
| A、常温下pH=5的CH3COOH溶液和pH=5的NH4Cl溶液中,水的电离程度前者比后者大 |
| B、用饱和Na2CO3溶液处理BaSO4沉淀,可将BaSO4转化为BaCO3 |
| C、BaSO4(s)+4C(s)═BaS(s)+4CO(g)室温下不能自发进行,说明该反应的△H<0 |
| D、为准确测定盐酸与氢氧化钠溶液反应的中和热,所用酸和碱的物质的量应相等 |


 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案科目:高中化学 来源: 题型:
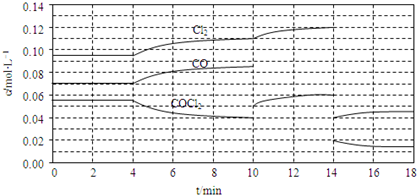
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
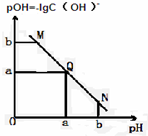 某温度下,向一定体积0.1mol/L醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中pOH与pH的变化关系如图所示,则正确的是( )
某温度下,向一定体积0.1mol/L醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中pOH与pH的变化关系如图所示,则正确的是( )| A、M点所示溶液导电能力强于Q点 |
| B、N点所示溶液中c(Na+)>c(CH3COO-) |
| C、M点和N点所示溶液中水的电离程度相同 |
| D、Q点消耗NaOH溶液的体积等于醋酸溶液的体积 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、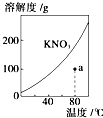 如图表示KNO3的溶解度曲线,图中a点所示的溶液是80℃时KNO3的不饱和溶液 |
B、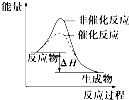 如图表示某放热反应分别在有、无催化剂的情况下反应过程中的能量变化 |
C、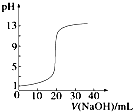 如图表示0.1000mol?L-1 NaOH溶液滴定20.00mL 0.1000mol?L-1醋酸溶液得到的滴定曲线 |
D、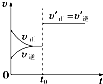 如图表示已达平衡的某反应,在t0时改变某一条件后反应速率随时间变化,则改变的条件可能是增大压强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某反应的反应过程中能量变化如图所示(图中E1 表示正反应的活化能,E2 表示逆反应的活化能).下列有关叙述正确的是( )
某反应的反应过程中能量变化如图所示(图中E1 表示正反应的活化能,E2 表示逆反应的活化能).下列有关叙述正确的是( )| A、催化剂能降低该反应的活化能 |
| B、逆反应的活化能大于正反应的活化能 |
| C、该反应为放热反应 |
| D、催化剂能改变该反应的焓变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、馒头、榨菜、黄瓜、香蕉 |
| B、面条、醋溜土豆丝、素炒白菜 |
| C、米饭、糖醋排骨、粉蒸肉、清蒸鲈鱼 |
| D、米饭、红烧鲫鱼、西红柿蛋汤、蒜蓉生菜、苹果 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温下,32g SO2含有NA个氧原子 |
| B、0.1mol?L-1的氨水含有0.1NA个OH- |
| C、常温常压下,22.4L CCl4含有个NA个CCl4分子 |
| D、1mol铁与足量氯气反应,转移2NA个电子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com