
【题目】下列关于化石燃料的加工说法正确的是( )
A. 石油裂化主要得到乙烯
B. 石油分馏是化学变化,可得到汽油、煤油
C. 煤干馏主要得到焦炭、煤焦油、粗氨水和焦炉气
D. 煤的气化是物理变化,是高效、清洁地利用煤的重要途径
科目:高中化学 来源: 题型:
【题目】将30.8g Al、Fe、Cu组成的合金溶于足量的NaOH溶液中,产生6.72L气体(标准状况)。另取等质量的该合金溶于过量的稀硝酸中,生成11.2L NO(标准状况),向反应后的溶液中加入足量的NaOH溶液,得到沉淀的质量为
A39.3g B.40.7g C.56.3g D.34.2g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚氯酸钠(NaClO2)是一种高效内氧化剂、漂白剂,其有效氯含量相当于漂白粉的7倍,主要用于棉纺、造纸业的漂白制,也用于食品消毒。水处理等。以氯酸纳等为原料制备亚氯酸钠的工艺流程如下:

已知:①亚氯酸钠(NaC1O2)受热易分解;
②NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO2·3H2O;
③ClO2常温下为黄绿色气体,纯ClO2易分解爆炸,一般用稀有气体或空气稀释到10% 以下更安全。
回答下列问题:
(1)在ClO2发生器中通入空气的作用是__________
(2)吸收塔中发生反应的化学方程式为:__________
(3)由滤液![]() NaClO2·3H2O,需采取的操作是在55C的条件下减压蒸发、_______、_______洗涤、干燥。工业上通常采用“减压蒸发”而不用“常压蒸发”,原因是_______;结晶后需要对晶体洗涤,为了减少损失,可以用______洗涤晶体。
NaClO2·3H2O,需采取的操作是在55C的条件下减压蒸发、_______、_______洗涤、干燥。工业上通常采用“减压蒸发”而不用“常压蒸发”,原因是_______;结晶后需要对晶体洗涤,为了减少损失,可以用______洗涤晶体。
(4)在碱性溶液中NaClO2比较稳定,在酸性溶液中, ClO2-和H+结合为HClO2,HClO2是唯一的亚卤酸,不稳定,易分解产生Cl2、ClO2和H2O,试写出HClO2分解的化学方程式___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家预言,末来最理想的燃料是绿色植物,即将植物的秸杆(主要成分是纤维素)在适当的催化剂存在下水解成葡萄糖,再将葡萄糖转化为乙醇,用作燃料。
(1)写出绿色植物的秸杆转化为乙醇的化学方程式:
①________________________________________________________________________;
②________________________________________________________________________。
(2)乙醇还可用于合成其他有机物,下图是用乙醇为起始原料合成环状酯D的框图,请在方框内填入相应有机物的结构简式:_______________。

(3)写出B+C→D的化学方程式:_______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于化学键的叙述 ,正确的一项是( )
A. 含有共价键的化合物一定是共价化合物
B. 单质分子中均不存在化学键
C. 含有分子间作用力的分子一定含有共价键
D. 离子化合物中一定含有离子键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA表示阿伏加德罗常数,下列叙述正确的是( )
A. 1 mol氨气中含共价键数均为4NA
B. 1 mol —OH中含有的电子数为9 NA
C. 1 mol Na2O2 固体中含离子总数为4 NA
D. 标准状况下,2.24 L CCl4所含分子数为0.1 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关等离子体的说法不正确的是 ( )
A.等离子体内部全部是带电荷的微粒
B.等离子体中正、负电荷大致相等
C.等离子体具有很好的导电性
D.等离子体用途十分广泛
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组将反应2KMnO4+10FeSO4+8H2SO4═2MnSO4+5Fe2(SO4)3+K2SO4+8H2O设计为如图原电池,其中甲、乙两烧杯中各物质的物质的量浓度均为2molL﹣1 , 溶液的体积均为200mL,盐桥中装有饱和K2SO4溶液.下列说法中错误的是( ) 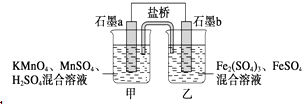
A.电池工作时,盐桥中的SO42﹣移向乙烧杯
B.石墨b的电极反应式为Fe2+﹣e﹣═Fe3+
C.当有0.1 mol SO42﹣进入烧杯时,反应消耗H+0.2 mol
D.当 MnSO4浓度变为2.2 molL﹣1时,反应中转移电子0.2 mol(不考虑溶液的体积变化)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com