
【题目】聚乙烯醇肉桂酸酯(M)可用作光刻工艺中的抗腐蚀涂层,其合成路线如下:
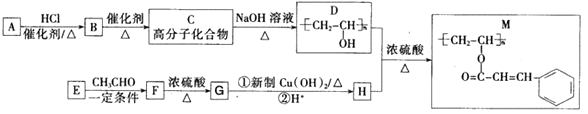
已知:

请回答:
(1)B的化学名称为_______________;M中含氧官能团的名称为_______________;F→G的反应类型为____________________。
(2)C→D的化学反应方程式为_________________________________________。
(3)E的结构简式为_______________;H的顺式结构简式为___________________。
(4)同时满足下列条件的F的同分异构体有_________种(不考虑立体异构):①属于芳香族化合物;②能发生水解反应和银镜反应。写出其中一种核磁共振氢谱有4种吸收峰,其峰面积之比为6:2:1:1的物质的结构简式_________。
(5)参照上述合成路线和相关信息,以乙烯和乙醛为原料(无机试剂任选)合成有机物![]() , 设计合成路线_____________。
, 设计合成路线_____________。
【答案】氯乙烯 酯基 消去反应 
![]()
 14
14 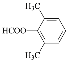 或
或 
![]()
【解析】
D和H发生酯化反应生成M,根据D和M结构简式知,H结构简式为![]() ;G发生氧化反应生成H,则G结构简式为
;G发生氧化反应生成H,则G结构简式为![]() ;F发生消去反应生成G,E发生加成反应生成F,则E、F结构简式为
;F发生消去反应生成G,E发生加成反应生成F,则E、F结构简式为![]() 、
、![]() ;A和HCl发生加成反应生成B,B发生加聚反应生成C,则C结构简式为
;A和HCl发生加成反应生成B,B发生加聚反应生成C,则C结构简式为 ,B结构简式为CH2=CHCl,A结构简式为HC≡CH。
,B结构简式为CH2=CHCl,A结构简式为HC≡CH。
(1)B的结构简式为CH2=CHCl,名称为氯乙烯;M中含氧官能团是酯基;F→G的反应为F发生消去反应生成G,故答案为:氯乙烯;酯基;消去反应;
(2)C→D的反应为 在氢氧化钠溶液中,加热发生水解反应生成
在氢氧化钠溶液中,加热发生水解反应生成![]() ,反应的化学方程式为
,反应的化学方程式为 ,故答案为:
,故答案为: ;
;
(3)E结构简式为![]() ;H结构简式为
;H结构简式为![]() ,具有顺反异构,顺式结构简式为
,具有顺反异构,顺式结构简式为 ,故答案为:
,故答案为:![]() ;
; ;
;
(4)F为![]() ,F的同分异构体符合下列条件:①属于芳香族化合物,说明含有苯环;②能发生水解反应和银镜反应,说明含有醛基和酯基,取代基为HCOO-和-CH2CH3有邻间对3种;如果取代基为HCOOCH2-和-CH3有邻间对3种;如果取代基为HCOOCH(CH3)-有1种;如果取代基为HCOOCH2CH2-有1种;如果取代基为-COOH和两个-CH3,两个甲基位于相邻物质,有2种;如果两个甲基位于间位,有3最后;如果两个甲基位于对位,有1种,符合条件的有14最后;其中核磁共振氢谱有4种吸收峰的物质的结构简式为
,F的同分异构体符合下列条件:①属于芳香族化合物,说明含有苯环;②能发生水解反应和银镜反应,说明含有醛基和酯基,取代基为HCOO-和-CH2CH3有邻间对3种;如果取代基为HCOOCH2-和-CH3有邻间对3种;如果取代基为HCOOCH(CH3)-有1种;如果取代基为HCOOCH2CH2-有1种;如果取代基为-COOH和两个-CH3,两个甲基位于相邻物质,有2种;如果两个甲基位于间位,有3最后;如果两个甲基位于对位,有1种,符合条件的有14最后;其中核磁共振氢谱有4种吸收峰的物质的结构简式为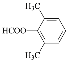 或
或 ,故答案为:14;
,故答案为:14;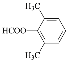 或
或 ;
;
(4)乙烯与溴的四氯化碳溶液发生加成反应生成1,2—二溴乙烷,1,2—二溴乙烷在氢氧化钠溶液中共热发生水解反应生成乙二醇,乙二醇氧化生成乙二醛,结合题给信息,乙二醛与乙醛反应生成![]() ,合成路线流程图为:
,合成路线流程图为: ![]() ,
,
故答案为:![]()


科目:高中化学 来源: 题型:
【题目】迷迭香酸具有抗氧化、延缓衰老、减肥降脂等功效,它的结构简式为:  ,以邻苯二酚为原料合成迷迭香酸的路线如下所示,下列说法错误的是
,以邻苯二酚为原料合成迷迭香酸的路线如下所示,下列说法错误的是

A. 有机物A分子中所有原子可能在同一平面上
B. 有机物B可以发生取代、加成、消去、氧化反应
C. 1molC在催化剂作用下,与H2加成最多可消耗8mol
D. 1molC与足量的NaOH溶液反应,最多可消耗6 molNaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】O3能吸收有害紫外线,保护人类赖以生存的空间。O3的分子结构如图,呈V形,两个键的夹角为116.5°,三个原子以一个O原子为中心,与另外两个O原子分别构成一个共价键;中间O原子提供两个电子,旁边两个O原子各提供一个电子,构成一个特殊的化学键——三个O原子均等地享有这些电子。请回答:

(1)臭氧与氧气互为________________。
(2)下列分子与O3分子的结构最相似的是________。
A. H2O B. CO2 C. SO2 D. BeCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某新型药物H( )是一种可用于治疗肿瘤的药物,其合成路线如图所示:
)是一种可用于治疗肿瘤的药物,其合成路线如图所示:

已知:(1)E的分子式为C9H8O2,能使溴的四氯化碳溶液褪色
(2)![]() (R为烃基)
(R为烃基)
(3)![]()
请回答下列问题:
(1)A的结构简式为_____;D的官能团的名称为_____。
(2)①的反应类型是_____;④的反应条件是_____。
(3)写出B→C的化学方程式_____。
(4)写出F+G→H的化学方程式_____。
(5)E有多种同分异构体,同时满足下列条件的E的同分异构体有_____种。
ⅰ.能发生银镜反应 ⅱ.能发生水解反应 ⅲ.分子中含的环只有苯环
(6)参照H的上述合成路线,设计一条由乙醛和NH2CH(CH3)2为起始原料制备医药中间CH3CONHCH(CH3)2的合成路线_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业锅炉内壁的水垢,不仅浪费燃料,而且容易引发安全隐患。某碳素钢锅炉水垢(主要成分有CaCO3、CaSO4、Mg(OH)2、Fe2O3、SiO2等)碱煮法清除的流程如下:

已知:20℃时几种难溶物的溶度积常数如下表(单位省略):

回答下列问题:
(1)“碱煮”环节,加入Na3PO4的主要目的是将CaSO4转化为Ca3(PO4)2,请写出该离子方程式______________________。
(2)“浸泡过程中,稀盐酸会溶解Fe2O3。溶解后的Fe2O3会加速锅炉腐蚀,故需“还原”处理。
①锅炉被加速腐蚀的原因是______________________;
②浸泡液还原”处理时,Sn2+转化为Sn4+,则反应中氧化剂与还原剂的物质的量之比为______________________。
(3)“钝化”处理的目的是在锅炉表面形成Fe3O4保护膜,同时生成可直接参与大气循环的气体。
①反应的离子方程式为_________________________________;
②为检验锅炉“钝化”处理后是否形成致密的保护膜,可往锅炉内壁刷上硫酸铜溶液。若观察到______________________(填现象),则保护膜致密性欠佳。
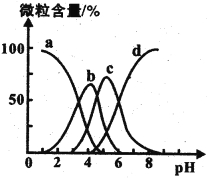
(4)柠檬酸(用H3R表示)可用作清除锅炉水垢的酸洗剂,溶液中H3R、H2R-、HR2-、R3-的含量与pH的关系如图所示。由此可推知,0.1 mol ·L-1 Na2HR溶液中各种阴离子浓度由大到小的排列顺序为______________________。
(5)用如图装置对锅炉用水(含Ca2+、Mg2+、HCO3-)进行预处理,可有效防止水垢形成。电解时,Ca2+形成沉淀的电极反应式为______________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子反应方程式正确的是
A. 实验室用固体氯化铵和熟石灰共热制取NH3:2NH4++Ca(OH)2![]() 2NH3↑+ Ca2++2H2O
2NH3↑+ Ca2++2H2O
B. 铜与浓硝酸反应: 3Cu + 8H+ + 2NO3-=3Cu2+ + 2NO↑ + 4H2O
C. 氨水与FeCl3溶液反应:3OH-+ Fe3+ =Fe(OH)3↓
D. Na2O2投入水中:2Na2O2+2H2O = 4Na++4OH-+O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室常用加热氯酸钾的方法制取少量氧气。
(1)请写出反应的化学方程式。_____
(2)现欲制取1.12L(标准状况)氧气,理论上需要消耗氯酸钾多少克?生成氯化钾物质的量多少?______、______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2016年IUPAC命名117号元素为TS(中文名![]() ,tián),TS的原子核外最外层电子数是7.下列说法不正确的是( )
,tián),TS的原子核外最外层电子数是7.下列说法不正确的是( )
A. TS是第七周期第ⅦA族元素 B. TS的同位素原子具有相同的电子数
C. TS在同族元素中非金属性最弱 D. 中子数为176的TS核素符号是![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知某盐酸溶液的密度为1.19g/cm3 ,质量分数为36.5%,则该溶液的物质的量浓度为___________
(2)含0.3 mol SO42-的Al2(SO4)3中所含的Al3+的数目为________________。
(3)相同质量的SO2、SO3硫原子的个数之比为_______________ 。
(4)33.3g某二价金属氯化物(ACl2)中含有0.6mol Cl,则ACl2的化学式是_________ 。
(5)标准状况下,1.204×1023个H2的体积约为_______________L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com