
| A、18g NH4+ 所含原子数为4NA |
| B、10g氖气所含原子数约为6.02×1023 |
| C、标准状况下,22.4L H2O所含的分子数为NA |
| D、常温常压下,32g O2和O3的混合气体所含原子数为2NA |
| m |
| M |
| m(O) |
| M(O) |
| 18g |
| 18g/mol |
| 10g |
| 20g/mol |
| m(O) |
| M(O) |
| 32g |
| 16g/mol |


 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案科目:高中化学 来源: 题型:
| A、Na2CO3、盐酸 |
| B、NaOH溶液、CO2 |
| C、NaHCO3溶液、石灰水 |
| D、Na2O2、CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用铜作电极电解饱和NaCl溶液,当线路中通过NA个电子时,阳极产生11.2L气体(标准状况下) |
| B、6.5g锌全部溶于一定量的浓硫酸,生成SO2与H2的混合气体,气体分子总数为0.1 NA |
| C、1.00 L 1.00 mol?L-1 Na2CO3溶液中,CO32-所带电荷总数为2NA |
| D、标准状况下,22.4 L HCl溶于水后溶液中含有nA个HCl分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、装置甲可用于蒸干NH4Cl饱和溶液制备NH4Cl |
| B、装置乙可用于实验室制备少量氢气、氯气等 |
| C、装置丙可用于实验室检验麦芽糖中是否含有醛基 |
| D、装置丁可用于实验室干燥并收集氨气,同时进行尾气处理,防止污染大气 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 按图甲装置进行实验,若图乙中横坐标X表示通过电极的电子的物质的量.下列叙述不正确的是( )
按图甲装置进行实验,若图乙中横坐标X表示通过电极的电子的物质的量.下列叙述不正确的是( )| A、F表示反应生成Cu的物质的量 |
| B、E表示反应消耗H2O的物质的量 |
| C、E表示反应生成O2的物质的量 |
| D、F表示反应生成H2SO4的物质的量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、白铁(镀锌铁)镀层破损后,先被腐蚀的是铁 |
| B、锌跟稀硫酸反应制取氢气,加入少量硫酸铜溶液能加快反应速率 |
| C、钢铁表面常易锈蚀生成Fe2O3?nH2O |
| D、金属的腐蚀主要是电化学腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、50×18×6.02×1023 |
| B、6.02×1023/50 |
| C、6.02×1023/50×18 |
| D、50×6.02×1023/18 |
查看答案和解析>>
科目:高中化学 来源: 题型:
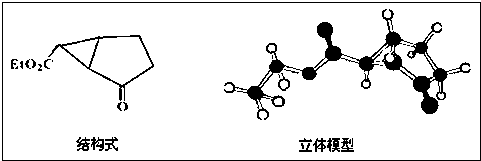
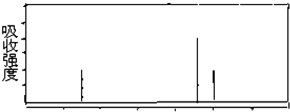
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com