
| A�� | �٢ۢ� | B�� | �٢� | C�� | �ڢ� | D�� | �ۢ� |
���� �پ������ᷴӦ���ɶ�����̼��
��̼�����Ƽ��ȷֽ⣬��̼���Ʋ��ܣ�
��̼�������Ȼ�����Ӧ���ɰ�ɫ��������̼�����Ʋ��ܣ�
����ͬŨ��ʱ��̼����ˮ��̶ȴ�
�ݾ���ʯ��ˮ��Ӧ����̼��Ƴ�����
��� �⣺�پ������ᷴӦ���ɶ�����̼��������ͬ�����ܹ۲��Ƿ�������ݼ��𣬹ʴ���
��̼�����Ƽ��ȷֽ⣬��̼���Ʋ��ܣ������ܲ���������ͨ�����ʯ��ˮ���۲����ް�ɫ���ǿɼ��𣬹���ȷ��
��̼�������Ȼ�����Ӧ���ɰ�ɫ��������̼�����Ʋ��ܣ���μ�BaCl2��Һ���۲����ް�ɫ���ǿɼ��𣬹���ȷ��
����ͬŨ��ʱ��̼����ˮ��̶ȴ���ǿ����ֱ����0.1mol•L-1����Һ���� pH���Ƚϴ�С�ɼ��𣬹���ȷ��
�ݾ���ʯ��ˮ��Ӧ����̼��Ƴ�������μӳ���ʯ��ˮ���۲����ް�ɫ���ǣ����ܼ��𣬹ʴ���
��ѡB��
���� ���⿼�����ʵļ���Ϊ��Ƶ���㣬�����ƵĻ��������ʡ������ķ�Ӧ��ʵ�鼼��Ϊ���Ĺؼ������ط�����ʵ�������Ŀ��飬ע��������ͬ���ܼ������ʣ���Ŀ�ѶȲ���


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | H2O��g���TH2��g��+$\frac{1}{2}$O2��g����H=+242 kJ•mol-1 | B�� | 2H2��g��+O2��g���T2H2O��l����H=-484 kJ•mol-1 | ||
| C�� | H2��g��+$\frac{1}{2}$O2��g���TH2O��g����H=-242 kJ•mol-1 | D�� | H2��g��+$\frac{1}{2}$O2��g���TH2O��l����H=-242 kJ•mol-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
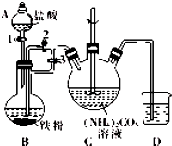 ��������{[CH3CH��OH��COO]2Fe}�㷺Ӧ��������Ʒ��Ӫ��Һ�ȣ�������ˮ������������FeCO3��Ӧ�Ƶã�
��������{[CH3CH��OH��COO]2Fe}�㷺Ӧ��������Ʒ��Ӫ��Һ�ȣ�������ˮ������������FeCO3��Ӧ�Ƶã��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Va=Vbʱ��c��CH3COO-��=c��K+�� | |
| B�� | Va��Vbʱ��c��CH3COOH��+c��H+��=c��OH-�� | |
| C�� | Va��Vbʱ��c��CH3COO-����c��K+����c��OH-����c��H+�� | |
| D�� | Va��Vb�����ʱ��c��K+��+c��H+��=c��OH-��+c��CH3COO-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 150 mL 3 mol•L-1�������Һ | B�� | 75 mL 3 mol•L-1�Ȼ�����Һ | ||
| C�� | 150 mL 3 mol•L-1�Ȼ�����Һ | D�� | 50 mL 3 mol•L-1�Ȼ�þ��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ǿ������Һ���ܴ������ڣ�Na+��K+��Cl-��HCO3- | |
| B�� | �������������Һ���д������ݲ�������Һ�У�Fe2+��Mg2+��NO3-��Cl- | |
| C�� | ���д���Fe3+����Һ�У�SCN-��I-��K+��Br- | |
| D�� | ��Һͨ����������������ӻ��ܴ������ڣ�K+��Na+��AlO2-��CO32- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��H1+��H2-��H3 | B�� | 2��H1+��H2+��H3 | ||
| C�� | ��H1+0.5��H2+��H3 | D�� | ��H1+0.5��H2+0.5��H3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ũ��Ϊ0.1 mol/L CH3COOH��0.1 mol/L CH3COONa��Ϻ���Һ�������ԣ���c��CH3COOH��c��Na+����c��CH3COO-�� | |
| B�� | ��ͬ�����£�pH=5�Ģ�NH4Cl��Һ����CH3COOH��Һ����ϡ����������Һ����ˮ�������c��H+�����٣��ڣ��� | |
| C�� | NaHCO3��Һ��c��OH-��-c��H+��=c����HCO3-��+2c��H2CO3�� | |
| D�� | �����ʵ���Ũ�ȵ�NaClO��NaHCO3�����Һ�У�c��HClO��+c��ClO-��=c��HCO3-��+c��H2CO3��+c��CO32-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NaCl�ĵ���ʽ�� | |
| B�� | ��ϩ�Ľṹ��ʽ��CH2CH2 | |
| C�� | Mgԭ�ӽṹʾ��ͼ�� | |
| D�� | �������ĵ��뷽��ʽ Fe2��SO4��3=2Fe3++3SO42�� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com