
| 物质 | X | Y | Z |
| 初始浓度/mol·L-1 | 0.1 | 0.2 | 0 |
| 平衡浓度/mol·L-1 | 0.05 | 0.05 | 0.1 |

 下列说法错误的是:
下列说法错误的是:

 A.反应达到平衡时,X的转化率为50%
A.反应达到平衡时,X的转化率为50% B.反应可表示为X+3Y
B.反应可表示为X+3Y 2Z,其平衡常数为1600
2Z,其平衡常数为1600 C.增大压强使平衡向生成Z的方向移动,平衡常数增大
C.增大压强使平衡向生成Z的方向移动,平衡常数增大 D.改变温度可以改变此反应的平衡常数
D.改变温度可以改变此反应的平衡常数科目:高中化学 来源:不详 题型:填空题
 B(g)+C(g),B的物质的量随时间的变化如图所示。 0—2min内的平均反应速率v(A)= . 相同温度下,若开始加入A(g)的物质的量是原来的2倍,则平衡时 是原来的2倍。
B(g)+C(g),B的物质的量随时间的变化如图所示。 0—2min内的平均反应速率v(A)= . 相同温度下,若开始加入A(g)的物质的量是原来的2倍,则平衡时 是原来的2倍。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.再滴加AgNO3溶液,观察是否有AgI沉淀产生 |
| B.加入CCl4振荡后,观察下层液体颜色 |
| C.加入CCl4振荡后,取上层清液,滴加AgNO3溶液,观察是否有AgCl沉淀产生 |
| D.加入CCl4振荡后,取上层清液,滴加KSCN溶液,观察是否有血红色 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 CH3OH(g)
CH3OH(g)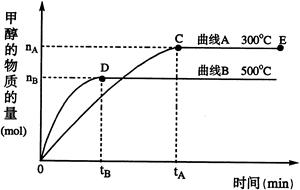
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
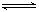 2Z(g)达到平衡的标志是
2Z(g)达到平衡的标志是 | A.Z生成的速率与X生成的速率相等 |
| B.单位时间生成a mol X,同时生成3a mol Y |
| C.X、Y、Z的浓度不再变化 |
| D.X、Y、Z的分子数比为1∶3∶2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2NH3(g)+ 92.4 kJ。实验测得起始、平衡时的有关数据如下表:
2NH3(g)+ 92.4 kJ。实验测得起始、平衡时的有关数据如下表:| 容器编号 | 起始时各物质的物质的量/mol[] | 平衡时反应中的能量变化 | ||
| N2 | H2 | NH3 | ||
| ① | 1 | 3 | 0 | 放出热量a kJ |
| ② | 2 | 3 | 0 | 放出热量b kJ |
| ③ | 2 | 6 | 0 | 放出热量c kJ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 qC(g)在密闭容器中进行。如图所示反应在不同时间t,温度T和压强P与反应物B的体积分数的关系曲线。根据图象填空
qC(g)在密闭容器中进行。如图所示反应在不同时间t,温度T和压强P与反应物B的体积分数的关系曲线。根据图象填空
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.②③ | B.②④ | C.①③ | D.①④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 Ag2O(s)+SO3(g),2SO3(g)
Ag2O(s)+SO3(g),2SO3(g) 2SO2(g)+O2(g)。10min后反应达到平衡,此时c(SO3)为0.4mol·L-1、c(SO2)为0.1mol·L-1,则下列叙述中不正确的是( )
2SO2(g)+O2(g)。10min后反应达到平衡,此时c(SO3)为0.4mol·L-1、c(SO2)为0.1mol·L-1,则下列叙述中不正确的是( )| A.SO3的分解率为20% |
| B.容器内气体的密度为40g/L |
| C.达到平衡时分解的Ag2SO4固体为0.5mol |
| D.10min内用O2表示的该反应的反应速率为0.005mol/(L·min) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com