
下列实验能达到预期目的的是( )
① 用硝酸钡溶液鉴别硫酸根离子与亚硫酸根离子;
②用溴水检验汽油中是否含有不饱和链烃;
③用乙醇从碘水中萃取碘;
④用盐析方法分离提纯蛋白质;
⑤用加热方法提纯含有少量碳酸氢钠的碳酸钠固体;
⑥闻氯气的气味时,用手轻轻在瓶口扇动,仅使极少量的氯气飘进鼻孔
A.②④⑤⑥ B.①③⑥ C.①②④⑤⑥ D.②③④⑤
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
固体单质A和气体单质B在容积一定的密闭容器中恰好完全反应生成气体C,相同温度下测得容器内压强不变,若产物气体C的密度是原气体密度的4倍,则判断正确的是
A. 单质A、B的摩尔质量之比是1∶4
B. 反应前后的气体质量之比一定是1∶4
C. 生成物C中,A的质量分数为50%
D. 生成物C中A、B两元素的原子个数比为3:1
查看答案和解析>>
科目:高中化学 来源: 题型:
要除去碳酸氢钠溶液中混有的少量碳酸钠,最好采用
A.加入过量的澄清石灰水 B.加入适量的氢氧化钠溶液
C.将溶液加热蒸干并灼烧 D.通入足量的CO2气体
查看答案和解析>>
科目:高中化学 来源: 题型:
向NaBr、NaI、Na2SO3混合溶液中通入过量的Cl2后,将溶液蒸干并充分灼烧,得到固体剩余物的组成可能是
A.NaCl Na2SO4 B.NaCl Na2SO4 NaBr
C.NaCl Na2SO4 I2 D.NaCl Na2SO4 NaI
查看答案和解析>>
科目:高中化学 来源: 题型:
化学与工农业生产和人类生活密切相关。下列说法中,不正确的是( )
A.油脂在碱性条件下水解可制得肥皂
B.海轮外壳上镶入锌块,可减缓船体的腐蚀
C.人体中缺碘元素会得贫血病
D.研制推广甲醇燃料汽车,有利于“减排目标”的实现
查看答案和解析>>
科目:高中化学 来源: 题型:
高铁酸钾(K2FeO4)和二氧化氯(ClO2)都是高效水处理剂,其工业制备的反应原理分别为 2Fe(OH)3+3 KClO+4KOH=2K2FeO4+3KCl+5H2O
2KClO3+ Na2SO3 +H2SO4=2ClO2 + Na2SO4 + K2SO4+ H2O
下列说法中,正确的是
A.上述两个反应中, KClO3做氧化剂,KClO 做还原剂
B.ClO2做水处理剂原理和明矾相同
C.K2FeO4用于杀菌后其还原产物还可用作净水剂
D.制备等物质的量的K2FeO4和ClO2,转移的电子数之比为1 : 1
查看答案和解析>>
科目:高中化学 来源: 题型:
“低碳循环”已经引起了国民的重视,试回答下列问题:
(1)煤的气化和液化可以提高燃料的利用率。
已知25℃,101 时:
时:

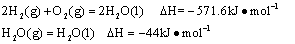
 则在25℃,101
则在25℃,101 时:
时: .
.
(2)高炉炼铁是CO气体的重要用途之一,其基本反应为:
已知在1100℃时,该反应的化学平衡常数K=0.263。
①温度升高,化学平衡移动后达到新的平衡,此时平衡常数K值 (填“增大”、“减小”或“不变”);
②1100℃时测得高炉时, ,在这种情况下,该反应是否处于化学平衡状态? (填“是”或“否”),其判断依据是 。
,在这种情况下,该反应是否处于化学平衡状态? (填“是”或“否”),其判断依据是 。
③目前工业上可用 来生产燃料甲醇,有关反应为:
来生产燃料甲醇,有关反应为:
 。现向体积为1L的密闭容器中,充入1mol
。现向体积为1L的密闭容器中,充入1mol 和3mol
和3mol ,反应过程中测得
,反应过程中测得 和
和 (g)的浓度随时间的变化如图所示。
(g)的浓度随时间的变化如图所示。
Ⅰ、从反应开始到平衡,氢气的平均反应速率 ;
;
Ⅱ、下列措施能使 增大的是 (填符号)。
增大的是 (填符号)。
 A.升高温度 B.再充入
A.升高温度 B.再充入
C.再充入 D.将
D.将 (g)从体系中分离
(g)从体系中分离
E.充入He(g),使体系压强增大
查看答案和解析>>
科目:高中化学 来源: 题型:
同一周期X、Y、Z三种元素,已知最高价氧化物对应水化物的酸性是HXO4>H2YO4>H3ZO4,则下列判断错误的是 ( )
A、原子半径X>Y>Z B、气态氢化物的稳定性HX>H2Y>ZH3
C、非金属性X>Y>Z D、阴离子的还原性Z3->Y2->X-
查看答案和解析>>
科目:高中化学 来源: 题型:
将1molI2(g)和2molH2(g)置于2L密闭容器中,在一定温度下发生反应:I2(g)+H2(g)  2HI(g) DH<0,并达到平衡。HI的体积分数j(HI) 随时间的变化如曲线(II)所示。
2HI(g) DH<0,并达到平衡。HI的体积分数j(HI) 随时间的变化如曲线(II)所示。
(1)达到平衡后,I2(g)的物质的量浓度为 ;
(2)若改变反应条件,j(HI)的变化过程如曲线(Ⅰ)所示,则该条件可能是 (填入下列条件的序号)。
①恒容条件下,升高温度
②恒容条件下,降低温度
③恒温条件下,缩小反应容器体积
④恒温条件下,扩大反应容器体积
⑤恒温、恒容条件下,加入适当的催化剂

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com