
(10分)二氧化氯![]() 是一种在水处理等方面有广泛应用的高效安全消毒剂。与
是一种在水处理等方面有广泛应用的高效安全消毒剂。与![]() 相比,
相比,![]() 不但具有更显著地杀菌能力,而且不会产生对人体有潜在危害的有机氯代物。
不但具有更显著地杀菌能力,而且不会产生对人体有潜在危害的有机氯代物。
![]() (1)在
(1)在![]() 的制备方法中,有下列两种制备方法:
的制备方法中,有下列两种制备方法:
![]() 方法一:
方法一:![]() ====
====![]()
![]() 方法二:
方法二:![]() ====
====![]()
![]() 用方法二制备的
用方法二制备的![]() 更适合用于饮用水的消毒,其主要原因是 。
更适合用于饮用水的消毒,其主要原因是 。
![]() (2)用
(2)用![]() 处理过的饮用水(
处理过的饮用水(![]() 为5.5~6.5)常含有一定量对人体不利的亚氯酸根离子
为5.5~6.5)常含有一定量对人体不利的亚氯酸根离子![]() .2001年我国卫生部规定,饮用水
.2001年我国卫生部规定,饮用水![]() 的含量应不超过0.2
的含量应不超过0.2![]() 。
。
![]() 饮用水中
饮用水中![]() 、
、![]() 的含量可用连续碘量法进行测定。
的含量可用连续碘量法进行测定。![]() 被
被![]() 还原为
还原为![]() 、
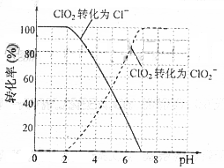
、![]() 的转化率与溶液PH的关系如右图所示。当
的转化率与溶液PH的关系如右图所示。当![]() 时,
时,![]() 也能被
也能被![]()
![]()
 完全还原成
完全还原成![]() 。反应生成的
。反应生成的![]() 用标准
用标准![]() 溶液滴定:
溶液滴定:
![]()
![]() ====
====![]()
![]() ① 请写出
① 请写出![]() 时,
时,![]() 与
与![]() 反应的离子方程式 。
反应的离子方程式 。
![]() ②请完成相应的实验步骤:
②请完成相应的实验步骤:
![]() 步骤1:准确量取
步骤1:准确量取![]() 水样加入到锥形瓶中。
水样加入到锥形瓶中。
![]() 步骤2:调节水样的
步骤2:调节水样的![]() 为7.0~8.0
为7.0~8.0
![]() 步骤3:加入足量的
步骤3:加入足量的![]() 晶体。
晶体。
![]() 步骤4:加少量淀粉溶液,用
步骤4:加少量淀粉溶液,用![]()
![]()
![]() 溶液滴定至终点,消耗
溶液滴定至终点,消耗![]() 溶液
溶液![]() .
.
![]() 步骤5: 。
步骤5: 。
![]() 步骤6;再用
步骤6;再用![]()
![]()
![]() 溶液滴定至终点,消耗
溶液滴定至终点,消耗![]() 溶液
溶液![]() 。
。
![]() ③根据上述分析数据,测得该引用水样中的
③根据上述分析数据,测得该引用水样中的![]() 的浓度为
的浓度为 ![]() (用含字母的代数式表示)。
(用含字母的代数式表示)。
![]() ④若饮用水中
④若饮用水中![]() 的含量超标,可向其中加入适量的,该反应的氧化产物是 (填化学式)
的含量超标,可向其中加入适量的,该反应的氧化产物是 (填化学式)
科目:高中化学 来源:2014届河北省高三上学期二调考试化学试卷(解析版) 题型:填空题
用二氧化氯(ClO2)、铁酸钠(Na2FeO4摩尔质量为166 g·mol-1)等新型净水剂替代传统的净水剂Cl2对淡水进行消毒是城市饮用水处理新技术。ClO2和Na2FeO4在水处理过程中分别被还原为Cl-和Fe3+。
(1)如果以单位质量的氧化剂所得到的电子数来表示消毒效率,那么ClO2、Na2FeO4、Cl2三种消毒杀菌剂的消毒效率由大到小的顺序是 > > 。(填化学式)
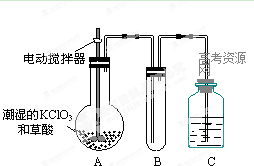
(2)二氧化氯是一种黄绿色有刺激性气味的气体,其熔点为-59℃,沸点为11.0℃,易溶于水。工业上用稍潮湿的KClO3和草酸在60℃时反应制得。某学生用如上图所示的装置模拟工业制取及收集ClO2,其中A为ClO2的发生装置,B为ClO2的凝集装置,C为尾气吸收装置。请问:
①A中反应还原剂与氧化剂的物质的量之比为1:2,该反应的化学方程式为 。
A部分还应添加温度控制(如水浴加热)装置,B部分还应补充什么装置: ;
②该装置按①补充完整后,装置A、B、C中还有一处设计明显不合理的是 _
(填“A、B或C”),理由是
③C中的试剂为NaOH溶液,反应时生成氯酸钠和亚氯酸钠(NaClO2),发该反应的离子方程式为 。若实验时需要450mL 4mol/L的NaOH溶液,则在精确配制时,需要称取NaOH的质量是 g,所使用的仪器除托盘天平、量筒、胶头滴管、玻璃棒外,还必须有 。
查看答案和解析>>
科目:高中化学 来源:2010-2011学年浙江省杭州萧山三校高三上学期期中联考化学试卷 题型:填空题
用二氧化氯(ClO2)、铁酸钠(Na2FeO4摩尔质量为166 g·mol-1)等新型净水剂替代传统的净水剂Cl2对淡水进行消毒是城市饮用水处理新技术。ClO2和Na2FeO4在水处理过程中分别被还原为Cl-和Fe3+。
(1)如果以单位质量的氧化剂所得到的电子数来表示消毒效率,那么,ClO2、Na2FeO4、Cl2三种消毒杀菌剂的消毒效率由大到小的顺序是 ▲ > ▲ > ▲ 。
(2)铁酸钠之所以能净水,除它本身具有强氧化性外,另一个原因可能是 ▲
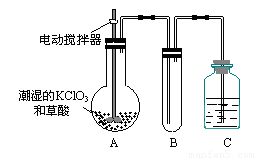
(3)二氧化氯是一种黄绿色有刺激性气味的气体,其熔点为-59℃,沸点为11.0℃,易溶于水。ClO2可以看做是亚氯酸(HClO2)和氯酸(HClO3)的混合酸酐。工业上用稍潮湿的KClO3和草酸在60℃时反应制得。某学生用如上图所示的装置模拟工业制取及收集ClO2,其中A为ClO2的发生装置,B为ClO2的凝集装置,C为尾气吸收装置。请问:
①A部分还应添加温度控制(如水浴加热)装置,B部分还应补充什么装置 ▲ ;
②该装置按①补充完整后,装置A、B、C中还有一处设计明显不合理的是 ▲ _(填“A、B或C”),理由是 ▲
③C中应装的试剂为 ▲ 。
C中发生反应的离子方程式为: ▲ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
作为世界卫生组织(WHO)推荐的A1级广谱、安全、高效消毒剂,二氧化氯(ClO2)在水处
| 理领域有着广泛应用。与氯气相比,它不但具有更显著的杀菌能力,而且不会产生对人体有潜在危害的有机氯代物。 (1)反应时,ClO2生成ClO2—、Cl—的转化率与溶液的pH的关系如图所示。则pH= 8时,ClO2被还原为_____________。 |
|
(2)亚氯酸根离子(ClO2—)对人体不利。欲在弱碱性条件下将水中的ClO2—转化为Cl—除去,若该反应体系中的物质有:NaClO2、Fe(OH)3、NaHCO3、FeCl2、NaCl、H2O、CO2。写出、配平有关化学方程式,并标出电子转移的方向和数目:
_____________________________________________________________________________。
(3)以下是ClO2的两种制备方法:
方法一:2NaClO3 + 4HCl → 2ClO2↑+ Cl2↑+ 2NaCl + 2H2O
方法二:2NaClO3 + H2O2 + H2SO4→ 2ClO2↑+ O2↑+ Na2SO4 + 2H2O
① 方法一,当有0.2mol电子发生转移时,参与反应的还原剂为_________mol。
② 方法二:该反应中H2O2_________(填序号)。
a. 发生氧化反应 b. 仅做氧化剂 c. 既被氧化又被还原 d. 既未被氧化也未被还原
③ 用方法二制备的ClO2更适合用于饮用水的消毒,其主要原因是___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
用二氧化氯(ClO2)、铁酸钠(Na2FeO4摩尔质量为166 g·mol-1)等新型净水剂替代传统的净水剂Cl2对淡水进行消毒是城市饮用水处理新技术。ClO2和Na2FeO4在水处理过程中分别被还原为Cl-和Fe3+。
(1)如果以单位质量的氧化剂所得到的电子数来表示消毒效率,那么ClO2、Na2FeO4、Cl2三种消毒杀菌剂的消毒效率由大到小的顺序是 > > 。(填化学式)

(2)二氧化氯是一种黄绿色有刺激性气味的气体,其熔点为-59℃,沸点为11.0℃,易溶于水。工业上用稍潮湿的KClO3和草酸在60℃时反应制得。某学生用如上图所示的装置模拟工业制取及收集ClO2,其中A为ClO2的发生装置,B为ClO2的凝集装置,C为尾气吸收装置。请问:
①A中反应还原剂与氧化剂的物质的量之比为1:2,该反应的化学方程式为 。
A部分还应添加温度控制(如水浴加热)装置,B部分还应补充什么装置: ;
②该装置按①补充完整后,装置A、B、C中还有一处设计明显不合理的是 _
(填“A、B或C”),理由是
③C中的试剂为NaOH溶液,反应时生成氯酸钠和亚氯酸钠(NaClO2),发该反应的离子方程式为 。若实验时需要450mL 4mol/L的NaOH溶液,则在精确配制时,需要称取NaOH的质量是 g,所使用的仪器除托盘天平、量筒、胶头滴管、玻璃棒外,还必须有 。
查看答案和解析>>
科目:高中化学 来源:2010上海虹口区高三二模 题型:填空题
作为世界卫生组织(WHO)推荐的A1级广谱、安全、高效消毒剂,二氧化氯(ClO2)在水处
|
理领域有着广泛应用。与氯气相比,它不但具有更显著的杀菌能力,而且不会产生对人体有潜在危害的有机氯代物。 (1)反应时,ClO2生成ClO2—、Cl—的转化率与溶液的pH的关系如图所示。则pH= 8时,ClO2被还原为_____________。 |
|
(2)亚氯酸根离子(ClO2—)对人体不利。欲在弱碱性条件下将水中的ClO2—转化为Cl—除去,若该反应体系中的物质有:NaClO2、Fe(OH)3、NaHCO3、FeCl2、NaCl、H2O、CO2。写出、配平有关化学方程式,并标出电子转移的方向和数目:
_____________________________________________________________________________。
(3)以下是ClO2的两种制备方法:
方法一:2NaClO3 + 4HCl → 2ClO2↑+ Cl2↑+ 2NaCl + 2H2O
方法二:2NaClO3 + H2O2 + H2SO4 → 2ClO2↑+ O2↑+ Na2SO4 + 2H2O
① 方法一,当有0.2mol电子发生转移时,参与反应的还原剂为_________ mol。
② 方法二:该反应中H2O2_________(填序号)。
a. 发生氧化反应 b. 仅做氧化剂 c. 既被氧化又被还原 d. 既未被氧化也未被还原
③ 用方法二制备的ClO2更适合用于饮用水的消毒,其主要原因是___________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com