
【题目】下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。试回答下列问题:

(1)写出元素k的基态原子的电子排布式________________________________,其原子核外有________个未成对电子。
(2)单质c在空气中充分燃烧的产物的分子构型为________ ,中心原子的杂化方式为_______,该分子含有________(填“极性键”或“非极性键”),该分子是________分子(填“极性”或“非极性”)。
(3)上述元素的最高价氧化物的水化物中,酸性最强的是___________________,碱性最的___________________(填化学式)。(每空1分)
(4)d的气态氢化物与d的最高价氧化物的水化物反应的离子方程式是:___________________________________________________________________________________________________________________________________。
(5)o、p两元素的部分电离能数据列于下表:比较两元素的I2、I3可知,气态o2+再失去一个电子比气p2+再失去一个电子困难。对此,你的解是__________________________________________________________________________。
元素 | o | P | |
电离能/kJ·mol-1 | I1 | 717 | 759 |
I2 | 1509 | 1561 | |
I3 | 3248 | 2957 | |

(6)短周期某主族元素的电离能情况如上图所示,则元素是上述周期表的__________元素(填元素符号)。
【答案】 1s22s22p63s23p4 2个 直线形 sp 极性键 非极性 HClO4 KOH NH3 + H+ =NH4+ Mn2+的3d轨道电子排布为半满状态,比较稳定 Al
【解析】根据元素周期表可知a为H元素、b为Li元素、c为C元素、d为N元素、e为O元素、f为F元素、g为Na元素、h为Mg元素、i为Al元素、j为Si元素、k为S元素、l为Cl元素、m为Ar元素、n为K元素、o为Mn元素、p为Fe元素;
(1)S元素的核电荷数为16,其基态原子的电子排布式为1s22s22p63s23p4,其原子核外p轨道上2个未成对电子;
(2)C原子价层电子对数=2+![]() =2,无孤对电子,中心原子的杂化方式为sp2,CO2分子构型为直线型,分子结构对称,正负电荷重心重合,为非极性分子;
=2,无孤对电子,中心原子的杂化方式为sp2,CO2分子构型为直线型,分子结构对称,正负电荷重心重合,为非极性分子;
(3)上述元素中非金属性F>Cl>S,F无正价,则最高价氧化物的水化物中酸性最强的是HClO4;K是最活泼的金属,则最高价氧化物的水化物中碱性最强的是KOH;
(4)NH3与HNO3生成NH4NO3,发生反应的离子方程式是NH3 + H+ =NH4+ ;
(5)p为Fe元素,o为Mn元素,Mn2+的3d轨道电子排布为半满状态较稳定,而Fe2+的3d轨道电子数为6,不是较稳定状态,所以气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难;
(6)根据表中所列的某主族元素的电离能可知,该元素原子最外层电子数为3,所以该元素为Al元素。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】不用其他试剂,用最简单的方法鉴别下列物质,正确的鉴别顺序是
①NaOH溶液;②Mg(NO3)2溶液;③CuSO4溶液;④KCl溶液。
A.①②③④ B.③④②① C.④①②③ D.③①②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、X、Y、Z、Q、R、T分别代表原子序数依次增大的短周期元素。元素A是原子半径最小的元素;X、Y、Z同周期且相邻,都是蛋白质的组成元素;X、R同族,Q与T原子的最外层电子数之和是R原子最外层电子数的2倍,T单质为淡黄色固体。U是d区元素,U2+的核外最高能级有2对成对电子。请回答下列问题:
(1)Y元素在周期表中的位置____________,位于周期表_____区;Q原子的核外电子排布式为________。
(2)X、Y、Z元素的第一电离能由大到小的顺序是________________。
(3)TZ3分子为________分子(填“极性”或“非极性”),YZ2-离子的VSEPR模型名称是________。(每空2分)
(4)Z和T的简单气态氢化物稳定性好的是_______(填化学式),原因是________________________________________________________________。
(5)A、X、Z、可形成分子式为A2XZ的有机物,则该化合物分子中B原子的轨道杂化类型是________;1mol该分子中含有π键的数目是________。
(6)通常情况下,U2+的溶液很稳定,它与YH3形成的配位数为6的配离子却不稳定,在空气中易被氧化为配位数不变的+3价配离子.该反应的离子方程式是________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】第四周期的Cr、Fe、Co、Ni、Cu、Zn等许多金属能形成配合物。
(1)Cr3+的核外电子排布式为____________________, 配离子[Cr(H2O)6] 3+中,与Cr3+形成配位键的原子是________(填元素符号)。
(2)NH3是一种很好的配体,氨分子是____________(填“极性”或“非极性”)分子,NH3的沸点_____________(填“高于”、“等于”或“低于”)AsH3。
(3)科学家通过X-射线测得胆矾(CuSO4·5H2O)的结构示意图可简单表示如下:
图中虚线表示的作用力为_______________________;
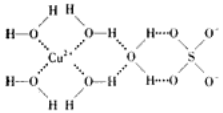
(4)胆矾溶液与氨水在一定条件下可以生成Cu(NH3)4SO4·H2O晶体。在Cu(NH3)4SO4·H2O晶体中,[Cu(NH3)4]2+为平面正方形结构,呈正四面体结构的原子团是_________,其中心原子的杂化类型是______。
(5)金属镍粉在CO气流中轻微加热,生成无色挥发性液态Ni(CO)4,呈正四面体构型。Ni(CO)4易溶于_________(填标号)。
A.水 B.四氯化碳 C.苯 D.硫酸镍溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知2-丁烯有顺、反两种异构体,在某条件下两种气体处于平衡,下列说法正确的是 ( )
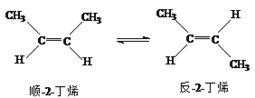 △H= -4.2 kJ/mol
△H= -4.2 kJ/mol
A. 反-2-丁烯和顺-2-丁烯具有相同的熔沸点。
B. 顺-2-丁烯比反-2-丁烯更稳定。
C. 加压和降温有利于平衡向生成顺-2-丁烯反应方向移动
D. 反-2-丁烯和顺-2-丁烯的核磁共振氢谱都有两个峰。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一小块钠投入盛有5mL饱和CuSO4溶液的试管里,不可能观察到的现象是( )
A.钠熔成小球并在液面上游动 B.有气体生成
C.试管底部有红色物质生成 D.溶液变浑浊
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是A、B、C、D四种有机物的有关信息:
A | ①能使溴的四氯化碳溶液褪色;②比例模型为 |
B | ①由C、H两种元素组成;②球棍模型为 |
C | ①由C、H、O三种元素组成;②能与Na反应,但不能与NaOH溶液反应;③能与D反应生成相对分子质量为88的酯 |
D | ①由C、H、O三种元素组成;②球棍模型为 |
回答下列问题:
(1)A与溴的四氯化碳溶液反应的化学方程式为:___________________。
(2)B具有的性质是________(填序号)。
①无色无味液体 ②有毒 ③不溶于水 ④密度比水大
⑤与酸性KMnO4溶液和溴水反应褪色 ⑥任何条件下不与氢气反应
(3)B在50~60℃时,能与混酸(浓硫酸和浓硝酸的混合溶液)反应,该反应的反应类型是_______________,化学方程式为___________________。
(4)C与D反应生成有香味的物质的化学方程式为: _______________,该反应的反应类型是_______________。
(5)B与液溴及铁反应的化学方程式为:__________, 生成有机物的名称是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作和现象对应的结论错误的是
选项 | 实验操作和现象 | 结论 |
A | 向溶液X中滴加BaCl2溶液,有白色沉淀生成 | 溶液X中可能含有SO42- |
B | 物质的量之比为2:3的稀硝酸和稀硫酸
| 反应结束后,锥形瓶中溶液的溶质是CuSO4,集气瓶中收集到的气体是NO |
C | 向1mL浓度均为0.05mol·L-1NaCl、NaI的混合溶液中滴加2滴0.01mol·L-1AgNO3溶液,振荡,沉淀是黄色 | Ksp(AgCl)<Ksp(AgI) |
D | 室温下,用pH试纸测得0.1mol·L-1 NaHSO3溶液的pH约为5 | HSO3-的电离程度大于其水解程度 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com