
����Ŀ������(COCl2)��ũҩ��ҽҩ���������ϵȷ��涼�й㷺Ӧ�ã�����������Ϊ��ɫ�����и���ζ������ʱΪ����ɫҺ�壬��ѧ���ʲ��ȶ�����ˮѸ��ˮ�⣬�����Ȼ��⡣ijʵ��С����������ʵ��װ�úϳɹ��������ù�����Ũ��ˮ��Ӧ�Ʊ�����[CO(NH2)2]����Ҫʵ��װ��(�г�װ����ȥ)�������������£�
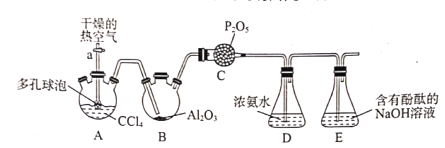
�ٰ���ͼ����װ�ã�����װ�õ������ԣ�Ȼ���װʵ��ҩƷ��
�ڴ���a.����A�л���ͨ�������ȿ�����
��һ��ʱ���װ��D����Һ����ֲַ������һ��Һ�Ϸ��д�����ɫ������
��֪��3CC14+Al2O3=3COCl2+2AlC13
�ش��������⣺
(1)��������װ�õ������Եķ�����___��
(2)�������ͨ�������ȿ���������Ϊ___��
(3)װ��C������___��
(4)װ��D�з�Ӧ����������[CO(NH2)2���⣬����NH4Cl���ɣ��÷�Ӧ�Ļ�ѧ����ʽΪ___����
(5)����װ��D�л��Һ�IJ�������Ϊ___��
(6)װ��E��������NaOH��Һ�������Ĺ�����Ӧ�����ӷ���ʽΪ��___��
(7)ʵ���D����Һ�������ᾧ�������ؽᾧ�ķ����õ����ؾ���(����������NH4Cl����)���ⶨ���þ��������صİٷֺ����ķ�������7.07g��������������ȫת��Ϊ�������ð�����100mL2.00molL-1��������Һ��ȫ���գ�ȡ����Һ10mL��0.4000molL-1���������Ʊ���Һ�ζ���
�ٵ���ζ��յ�ʱ��������������45.00mL����þ��������ص���������Ϊ___(����3λ��Ч����)��
�����ζ�ǰδ���������Ʊ���Һ��ϴ�ζ��ܣ����ø��徧�����ص���������___(ѡ����ƫ��������ƫС��)��
���𰸡��رջ���a����װ��ĩ�˵��ܲ���ʢˮ���ձ��У�����װ��A���۲�ĩ�˵��ܿ������ݲ�����ֹͣ���ȣ�ĩ�˵��ܿ���һ��ˮ�� ��������CCl4�����ҽ��ȵ�CC14�������������Bװ�÷�����Ӧ ��ֹDװ���е�ˮ����װ��B�����¹�������ˮ�ⷴӦ COC12+4NH3H2O=CO(NH2)2+2NH4Cl+4H2O ��Һ COCl2+4OH-=CO32-+2Cl-+2H2O 84.9% ƫС
��������
��ʵ��Ŀ���Ǻϳɹ��������ù�����Ũ��ˮ��Ӧ�Ʊ�����[CO(NH2)2]��������ѧ���ʲ��ȶ�����ˮѸ��ˮ�⣬�����Ʊ�����ʱҪ������ϵ����ø�����ȿ����������������Ȼ�̼�������䴵��Bװ������Al2O3���з�Ӧ�Ʊ�������Cװ�ÿ��Է�ֹˮ��������Bװ�ã�����ͨ��Ũ��ˮ�з�Ӧ�Ʊ�[CO(NH2)2]��D���б������������Ȼ�̼���������Ȼ�̼������ˮ�����Գ��ֲַ�����δ��Ӧ�Ĺ����ڻ��Һ�Ϸ���ˮ������Ӧ����HCl��CO2��HCl�����ӷ����İ�����Ӧ�����Ȼ�泥����Բ����������̣�װ��E��������β����
(7)�ζ�ԭ��Ϊ�Ƚ���Ʒ�е�NԪ��ȫ��ת��Ϊ�������������գ�Ȼ����NaOH��Һ�ζ�ʣ�������������Ӷ�ȷ��NԪ�ص������ٸ����غ㷨����ȷ����Ʒ�����صĺ�����
(1)����ͨ�����ȷ�����װ�õ������ԣ��������Ϊ���رջ���a����װ��ĩ�˵��ܲ���ʢˮ���ձ��У�����װ��A���۲�ĩ�˵��ܿ������ݲ�����ֹͣ���ȣ�ĩ�˵��ܿ���һ��ˮ����˵�����������ã�
(2)���ݷ�����֪ͨ������ȿ���������Ϊ��������CCl4�����ҽ��ȵ�CC14�������������Bװ�÷�����Ӧ��
(3)������ѧ���ʲ��ȶ�����ˮѸ��ˮ�⣬װ��C��������Ҫ�Ƿ�ֹDװ���е�ˮ��������װ��B�����¹�������ˮ�ⷴӦ��
(4)D�з�Ӧ��ΪCOCl2��һˮ�ϰ���������[CO(NH2)2]��NH4Cl�ȣ�����Ԫ���غ�ɵ÷���ʽΪCOC12+4NH3H2O=CO(NH2)2+2NH4Cl+4H2O��
(5)װ��D����Һ�ֲ㣬��ͨ����Һ�ķ������룻
(6)������ˮˮ�����HCl��CO2��HCl��NaOH��Ӧ����NaCl��ˮ��CO2��NaOH��Ӧ����Na2CO3��ˮ�����Թ�����NaOH��Һ��Ӧ�����ӷ���ʽΪCOCl2+4OH-=CO32-+2Cl-+2H2O��
(7)�ٵ���ζ��յ�ʱ��������������45.00mL����10mL����Һʣ��n(H+)=0.045L��0.4000mol/L=0.018mol�������õİ���n(NH3)=0.1L��2.00mol/L��2-![]() =0.22mol���辧����n([CO(NH2)2])=x mol��n(NH4+)=y mol��
=0.22mol���辧����n([CO(NH2)2])=x mol��n(NH4+)=y mol��
����Ԫ���غ�ɵ�![]() �����x=0.1mol��y=0.02mol���������ص���������Ϊ
�����x=0.1mol��y=0.02mol���������ص���������Ϊ![]() ��100%=84.9%��
��100%=84.9%��
�����ζ�ǰδ���������Ʊ���Һ��ϴ�ζ���,��ʹ���ĵ��������Ʊ���Һƫ�࣬���øþ��������ص���������ƫС��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ����50mL����0.1molCl2����ˮ�еμ�2mol��L1��NaOH��Һ���õ���ҺpH�����NaOH��Һ����ı仯��ͼ��ʾ������˵����ȷ����
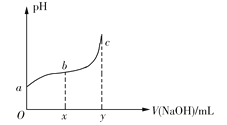
A.��a��pH=4����c(Cl)=mc(HClO)����HClO�ĵ���ƽ�ⳣ��Ϊ![]()
B.��x=100��b���Ӧ��Һ�У�c(OH)>c(H+)������pH��ֽ�ⶨ��pH
C.��y=200��c���Ӧ��Һ�У�c(OH)c(H+)=2c(Cl)+c(HClO)
D.b��c�Σ���NaOH��Һ�ĵ��룬![]() ������
������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1.12 g���ۼ���25 mL 2mol/L���Ȼ�����Һ�У���ַ�Ӧ��������
A. ����ʣ�࣬��Һ��dz��ɫ��Cl�� Ũ�Ȼ�������
B. ����Һ�е�����ɫKSCN��Һ���Ի�ɫ
C. ���������뻹ԭ��������ʵ���֮��Ϊ2��5
D. Fe2+��Fe3+�����ʵ���֮��Ϊ6��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪���ڱ�������(H2A)��Ka1��1.1��10��3��Ka2��3.9��10��6�������£���0.1 mol��L��1 NaOH��Һ�ζ�20 mL 0.1 mol��L��1�ڱ����������(KHA)��Һ������˵����ȷ����(����)
A.0.1 mol��L��1 KHA��Һ�У�c(K��)>c(HA��)��2c(A2��)
B.����NaOH��Һ��pH��8ʱ��c(K��)>c(A2��)>c(HA��)>c(H2A)
C.����20 mL NaOH��Һʱ��c(OH��)��c(A2��)��c(Na��)��c(H��)��c(H2A)
D.�ڵζ������У�ˮ�ĵ���̶�һֱ��С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����CO2Ӧ�����������ȼ�ϼ״������ܻ�������ЧӦ��Ӱ�죬����Ϊ��Դ���Ʊ������µ���������ϳɷ�ӦΪCO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)���ش��������⣺
CH3OH(g)+H2O(g)���ش��������⣺
��1����ͼΪCO2ƽ��ת���ʺ��¶ȡ�ѹǿ�Ĺ�ϵ������ѹǿ�ֱ�Ϊ3.0MPa��4.0MPa��5.0MPa����ͼ��֪���÷�ӦΪ_______________��Ӧ������ȡ�������")����CO2�ij�ʼŨ��ΪcomolL-1������5.0MPaʱ�����ݼ���÷�Ӧ��ƽ�ⳣ��K(240k)=_______________ (�г�����ʽ���ɣ�������4.0MPaʱ��СͶ�ϱȣ���CO2��ƽ��ת�������߿���λ��II�ߵ�_______________����Ϸ������·���)��

��2�����ö�����̼�Ƶõļ״���������ȡ�װ����䷴Ӧԭ��ΪCH3OH(g)+NH3(g)![]() CH3NH2(g)+H2O(g)��H����֪�÷�Ӧ����ػ�ѧ���ļ����������£�
CH3NH2(g)+H2O(g)��H����֪�÷�Ӧ����ػ�ѧ���ļ����������£�
���ۼ� | C��O | H��O | N��H | C��N |
����/k.Jmol-1 | 351 | 463 | 393 | 293 |
��÷�Ӧ�ġ�H=_______________k.Jmol-1 ��
��3����֪����CO(g)+NO2(g)![]() CO2(g)+NO(g) ��H1=-226kJrnol-1
CO2(g)+NO(g) ��H1=-226kJrnol-1
��N2(g)+2O2(g)![]() 2NO2(g)��H2=+68kJmol-1
2NO2(g)��H2=+68kJmol-1
��N2(g)+O2(g)![]() 2NO(g) ��H3=+183kJmol-1
2NO(g) ��H3=+183kJmol-1
��2CO(g)+2NO(g)![]() 2CO2(g)+N2(g) ��H=_______________kJmol-1��
2CO2(g)+N2(g) ��H=_______________kJmol-1��
��4��һ���¶��£����д�ʩһ���ܼӿ췴ӦCO2(g)+3H2��g)![]() CH3OH(g)+H2O(g)�����ʵ���_______________����ѡ����ĸ����
CH3OH(g)+H2O(g)�����ʵ���_______________����ѡ����ĸ����
A.��ʱ��ȥ�״� B.�Ľ����� C.��߷�Ӧ��Ũ�� D.��������ѹǿ
��5������������ѡ������NiO- Al2O3��Ϊ��������ҵ�ϳ���Ni(NO3)2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��pAg����lg c(Ag��)��Ksp(AgCl)��1��10��12����ͼ����10 mL AgNO3��Һ������0.1 mol/L��NaCl��Һʱ����Һ��pAg���ż���NaCl��Һ�����(��λ��mL)�仯��ͼ��(ʵ��)������ͼ���������н�����ȷ����

A. ԭAgNO3��Һ�����ʵ���Ũ��ΪҲΪ0.1 mol��L��1
B. ͼ��x�������Ϊ(10��6)
C. ͼ��x�����Ϊ��Һ��Ag����������ȫ
D. ��0.1 mol��L��1��NaCl����0.1 mol��L��1NaI����ͼ�����յ���Ϊ���߲���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����(Ni)�ϴ�������Ҫ����Ni��������Al��Al2O3��Fe�������������ᡢ������ʡ����ֽ�����������Ksp����ֵ���±���ʾ��
��ѧʽ | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Ni(OH)2 |
Ksp����ֵ | 10-17 | 10-39 | 10-34 | 10-15 |
���ú����ϴ����Ʊ�NiSO4��7H2O���壬������ͼ���£�
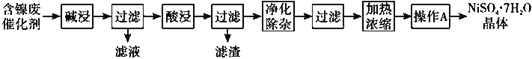
�ش��������⣺
��1���������ʱ������Ӧ�����ӷ���ʽΪ2A1+2OH-+2H2O=2AlO2��+3H2����_________��
��2�����������ʹ�õ���Ϊ_____________��
��3�������������������H2O2��Һ����������__________________________��Ȼ�����pHʹ��Һ����Ԫ��ǡ����ȫ��������ʱ��pHΪ____________������1λС������
��4��������A��Ϊ_____�����ˡ�ϴ�ӡ�������ò�Ʒ��
��5��NiSO4��NaOH��Һ�пɱ�NaClO����ΪNiOOH���÷�Ӧ�Ļ�ѧ����ʽΪ_______��
��6��NiOOH����Ϊ�����صĵ缫���ϣ��õ�صĹ���ԭ������ͼ��ʾ������ʱ�������ĵ缫��ӦʽΪ____________��
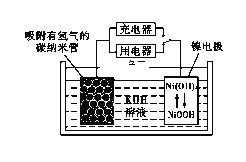
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2019��10��1�գ��ҹ��ɹ��ٰ������ʮ�����ı���������ı���ʽ�ϻ�϶�����������Դ���������࣬չʾ���ۺϹ����������Ƽ���չˮƽ��ͬʱҲ˵����Դ��ȱ������������ٵ��ش����⡣�״���һ�ֿ�������Դ�����й㷺�Ŀ�����Ӧ��ǰ����
��ҵ������Ȼ��Ϊԭ�ϣ���Ϊ�����Ʊ��״���
(i)�Ʊ��ϳ�����CH4(g)+H2O(g) CO(g)+3H2(g) ��H= +206.0kJmol-1
(ii)�ϳɼ״���CO(g)+2H2(g)CH3OH(g) ��H= -90.67kJmol-1
(1)�Ʊ��ϳ�������ҵ������Ϊ����ϳ�����H2������ CO ��������⣬ԭ������������CO2�������ķ�Ӧ(iii)��CO2(g)+H2(g) CO(g)+H2O(g) ��H= +41.17kJmol-1��Ϊ��ʹ�ϳ��������ѣ�������ԭ�����ж�����̼�����������Ϊ _______��
(2)Ϊ��Լ��ʯ��Դ������̼�ŷţ���CO2����CO��Ϊ�Ʊ��״���̼Դ����Ϊ��ǰ�о��Ľ��㡣
����д��������̼����ϳ�ˮ�����ͼ״����Ȼ�ѧ����ʽ____________��
���о������ڶ�����̼�ϳɼ״���ԭ�����ķ�Ӧ�У����������������䣬�����������������ִ�������Ӧ������ͬʱ���CO2��ת�����淴Ӧ��ϵ���¶ȱ仯��ͼ��ʾ��

a��d ���з�Ӧһ������ƽ��״̬�ĵ���____��CO2��ת���� a ��� c ��ߵ�ԭ���� ____��
�����������շ�ܷ��Ʊ��������������ڷ�չ�ǽ�������ʵ��CO2�����ԭ�Ʊ��״�����ȡ����Ҫ��չ���÷�Ӧ������ͼ��ʾ��
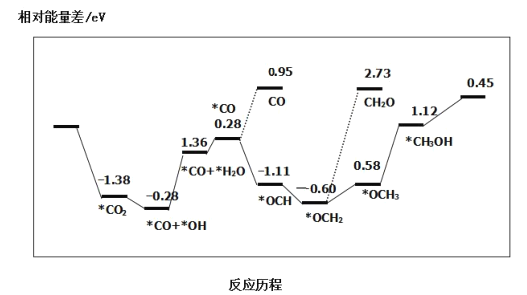
���õ��ĸ������� CO ��CH2O��������Խ��ٵĸ�����Ϊ___�������ϳɼ״��ķ�Ӧ���ʽ�����Ҫʹ��Ӧ���ʼӿ죬��Ҫ�������б仯��____(����ĸ)�������仯��
A��*CO �� *OCH B��*CO+*OH��*CO+*H2O
C��*OCH2��*OCH3D��*OCH3��*CH3OH
(3)��һ�ݻ��ɱ���ܱ������г���10molCO��20molH2�ϳɼ״���CO��ƽ��ת�������¶�(T)��ѹǿ(P)�ı仯��ͼ��ʾ��
���Ƚ�A��B ����ѹǿ��СPA_______PB�>��<�� =��)
�����ﵽ��ѧƽ��״̬ A ʱ�����������Ϊ 10 L�������Ӧ��ʼʱ�Գ��� 10molCO��20molH2������ƽ��״̬ B ʱ�����������V(B)=_______L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CO��NO��NO2��SO2���ж������Σ�����彡�����ƻ���������������������о�һֱ�ǿƼ����ע���ص㡣��ش��������⣺
��1������β���е�CO��NO��NO2���ж������Σ�����彡������������β���Ӵ�ת���������ж�����ת��Ϊ�����塣
��֪����2NO(g)��O2(g)=2NO2(g) ��H1=-112.3kJ��mol-1
��NO2(g)��CO(g)=NO(g)��CO2(g) ��H2=-234kJ��mol-1
��N2(g)��O2(g)=2NO(g) ��H3=��179.5kJ��mol-1
��д��CO��NO2��������Ⱦ������Ȼ�ѧ����ʽ__��
��2������CO��NO����ͬ����Ͷ��һ�ܱ������з�����Ӧ��2CO(g)��2NO(g)![]() N2(g)��2CO2(g) ��H=-759.8kJ��mol-1������Ӧ�ﵽƽ��ʱ�����õĻ�������к�N2�����������
N2(g)��2CO2(g) ��H=-759.8kJ��mol-1������Ӧ�ﵽƽ��ʱ�����õĻ�������к�N2�����������![]() �ı仯������ͼ1��
�ı仯������ͼ1��
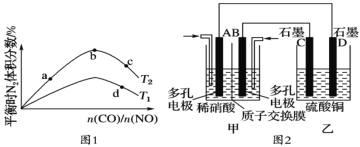
��a��b��c��d�ĵ��ƽ�ⳣ���Ӵ�С��˳��Ϊ__��
����![]() =0.8����Ӧ��ƽ��ʱ��N2���������Ϊ20%����NO��ת����Ϊ__��
=0.8����Ӧ��ƽ��ʱ��N2���������Ϊ20%����NO��ת����Ϊ__��
��3������NO2��O2ͨ�������Ƴ���ͼ2��ʾװ�ã�D�缫���к�ɫ������������A�缫�ĵ缫��ӦʽΪ__������һ��ʱ������������0.1molCu2(OH)2CO3��ʹ��Һ��ԭ����ת�Ƶĵ�����Ϊ__NA��
��4�������£�SO2�����ü���Һ���մ���������SO2ͨ�뵽NaOH��Һ�У���ַ�Ӧ��õ�amol��L-1��NaHSO3��Һ������Һ��pH=5�������Һ��c(SO32-)___c(H2SO3)������>������=��������������HSO3-�ĵ��볣��ԼΪ___���ú�a��ʽ�ӱ�ʾ����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com