
| A、XYZ3 |
| B、XYZ4 |
| C、XYZ |
| D、X2YZ3 |


科目:高中化学 来源: 题型:
| 实验编号 | ① | ② | ③ | ④ | ⑤ |
| C(I-)/mol?L-1 | 0.040 | 0.080 | 0.080 | 0.160 | 0.120 |
| C(S2O32-)/mol?L-1 | 0.040 | 0.040 | 0.080 | 0.020 | 0.040 |
| t/s | 88.0 | 44.0 | 22.0 | 44.0 | t2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、非金属性最强的元素,其最高价氧化物对应水化物的酸性最强 |
| B、碱金属随原子序数的增大,其半径逐渐增大 |
| C、在周期表中,族序数都等于该族元素的最外层电子数 |
| D、卤素元素随原子序数的增大,其得电子能力逐渐增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原子及其离子的核外电子层数等于该元素所在周期数 |
| B、元素周期表中第ⅦA元素的气态氢化物稳定性从上到下逐渐减弱 |
| C、最外层电子数是8的微粒都是稀有气体原子 |
| D、同一元素的各种同位素的物理性质和化学性质完全相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 原子序数 | 电子层数 | 最外层电子数 | 达到稳定状态时的最外层电子数 |
| 1-2 | 1 | 2 | |
| 3-10 | 2 | 8 | |
| 11-18 | 3 | 8 | |
| 结论:随着原子序数的递增,元素原子的 | |||
查看答案和解析>>
科目:高中化学 来源: 题型:
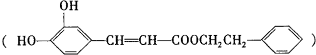 ,在一定条件下能发生如图所示的转化:
,在一定条件下能发生如图所示的转化: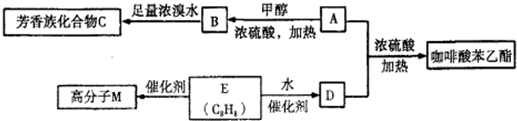
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com