
下列溶液或浊液中,关于离子浓度的说法正确的是
A.一定浓度的氨水加水稀释的过程中,c(NH4+)/ c(NH3·H2O)的比值减小
B.浓度均为0.1 mol·L-1的Na2CO3、NaHCO3混合溶液中:c(CO32-) > c(HCO3-),且2c(Na+)=3[c(CO32-)+c(HCO3-)]
C.0.2 mol·L-1的醋酸(CH3COOH)溶液与0.1 mol·L-1 NaOH溶液等体积混合后:c(CH3COO-) + 2c(OH-) = c(CH3COOH) + 2c(H+)
D.常温下,已知:Ksp(AgCl)=1.8×10-10,Ksp(Ag2Cr2O4)=2.0×10-12,则Ag2CrO4悬浊液中的c(Ag+)一定小于AgCl悬浊液中的c(Ag+)
C
【解析】
试题分析:A.一定浓度的氨水加水稀释的过程中,氢氧根浓度减小,根据电离常数可知c(NH4+)/ c(NH3·H2O)=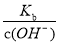 ,温度不变,电离常数不变,氢氧根浓度减小,则比值增大,A错误; B.浓度均为0.1 mol·L-1的Na2CO3、NaHCO3混合溶液中碳酸根的水解程度大于碳酸氢根,则c(CO32-)<c(HCO3-),由于不能确定二者的体积,则2c(Na+)=3[c(CO32-)+c(HCO3-)]是错误的,B不正确;C.0.2 mol·L-1的醋酸(CH3COOH)溶液与0.1 mol·L-1 NaOH溶液等体积混合后醋酸过量,根据电荷守恒c(CH3COO-) +c(OH-) = c(Na+) + c(H+)和物料守恒c(CH3COO-) +c(CH3COOH)=2c(Na+)可知,溶液中c(CH3COO-) + 2c(OH-)=c(CH3COOH) + 2c(H+),C正确;D.常温下,已知:Ksp(AgCl)=1.8×10-10,Ksp(Ag2Cr2O4)=2.0×10-12,当Ag2CrO4悬浊液中的c(Ag+)不一定小于AgCl悬浊液中的c(Ag+),还需要考虑阴离子的浓度,D错误,答案选C。
,温度不变,电离常数不变,氢氧根浓度减小,则比值增大,A错误; B.浓度均为0.1 mol·L-1的Na2CO3、NaHCO3混合溶液中碳酸根的水解程度大于碳酸氢根,则c(CO32-)<c(HCO3-),由于不能确定二者的体积,则2c(Na+)=3[c(CO32-)+c(HCO3-)]是错误的,B不正确;C.0.2 mol·L-1的醋酸(CH3COOH)溶液与0.1 mol·L-1 NaOH溶液等体积混合后醋酸过量,根据电荷守恒c(CH3COO-) +c(OH-) = c(Na+) + c(H+)和物料守恒c(CH3COO-) +c(CH3COOH)=2c(Na+)可知,溶液中c(CH3COO-) + 2c(OH-)=c(CH3COOH) + 2c(H+),C正确;D.常温下,已知:Ksp(AgCl)=1.8×10-10,Ksp(Ag2Cr2O4)=2.0×10-12,当Ag2CrO4悬浊液中的c(Ag+)不一定小于AgCl悬浊液中的c(Ag+),还需要考虑阴离子的浓度,D错误,答案选C。
考点:考查溶液中离子浓度大小比较


 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案科目:高中化学 来源:2014-2015北京市昌平区高一上学期期末考试化学试卷(解析版) 题型:选择题
下列关于Na2O和Na2O2 的说法中,正确的是
A.均能与水反应 B.氧元素的化合价均为-2
C.均为淡黄色固体 D.均能与CO2反应放出氧气
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市黄浦区高三上学期期末调研测试化学试卷(解析版) 题型:选择题
下列表达正确的是
A.氟原子中能量最髙的电子其电子云图:
B.CO2的分子模型示意图:
C.2-甲基丁醛的结构简式:
D.N2的结构式:
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省资阳市高三第二次诊断性考试理综化学试卷(解析版) 题型:选择题
在2 L的密闭容器中进行如下反应:CO(g)+H2O(g) CO2(g)+H2(g),有如下数据:
CO2(g)+H2(g),有如下数据:
实验 | 温度/℃ | 起始量/mol | 平衡量/mol | |||
CO | H2O | CO2 | H2 | CO2 | ||
1 | 650 | 2.0 | 1.0 | 0 | 0 | 0.8 |
2 | 800 | 2.0 | 2.0 | 0 | 0 | 1.0 |
下列说法正确的是
A.正反应为吸热反应
B.实验1中,CO的转化率为80%
C.650℃时,化学平衡常数K=
D.实验1再加入1.0 mol H2O,重新达到平衡时,n(CO2)为1.6 mol
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省眉山市高三第一次诊断性考试理综化学试卷(解析版) 题型:实验题
(14分)以铬铁矿(主要成分为FeO和Cr2O3 ,含有Al2O3、SiO2等杂质)为主要原料生产化工原料红矾钠(红矾钠的主要成分为重铬酸钠:Na2Cr2O7·2H2O),其主要工艺流程如下:

查阅资料得知:
i. 常温下,NaBiO3不溶于水,有强氧化性,在碱性条件下,能将Cr3+转化为CrO42-。
ii.
物质 | 开始沉淀的pH值 | 完全沉淀的pH值 |
Fe(OH)3 | 2.7 | 3.7 |
Al(OH)3 | 3.4 | 4.4 |
Cr (OH)3 | 4.6 | 5.9 |
Fe(OH)2 | 7.5 | 9.7 |
Bi(OH)3 | 0.7 | 4.5 |
回答下列问题:
(1)反应之前先将矿石粉碎的目的是 。
(2)操作I、III、IV用到的主要玻璃仪器有玻璃棒和__________(填仪器名称)。
(3)写出④反应的离子反应方程式 。
(4)⑤中酸化是使CrO42-转化为Cr2O72-,写出该反应的离子方程式 。
(5)将溶液H经过下列操作,蒸发浓缩,__________,过滤,洗涤,干燥即得红矾钠。
(6)取一定质量的固体D溶解于200mL的硫酸中,向所得溶液中加入5mol/L的NaOH溶液,生成沉淀的物质的量n与加入NaOH溶液的体积V关系如图所示,则硫酸的浓度为 ,固体D中含Fe化合物的物质的量为 。

查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省眉山市高三第一次诊断性考试理综化学试卷(解析版) 题型:选择题
化学与生活、社会密切相关,下列说法错误的是
A.过氧化钠可作航天员和潜水员的供氧剂
B.干冰和碘化银均可用于人工降雨
C.近年来出现的城市雾霾与汽车尾气的排放无关
D.高铁车厢大部分材料采用铝合金,因为铝合金强度大、质量轻、抗腐蚀能力强
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市静安区高三上学期期末考试化学试卷(解析版) 题型:填空题
(本题共12分)氢是宇宙中最丰富的元素,为一切元素之源。
23.H原子的电子排布式是“1s1”,该式子未表明电子运动状态的方面是 (选填编号)。
A.电子层 B.电子亚层
C.电子云的伸展方向 D.电子的自旋
24.金属锂与氢气在一定条件下能直接化合生成 LiH,以下事实能说明LiH是离子化合物的是 (选填编号)。
A.H为-1价 B.熔融状态能导电 C.加热到600℃不分解
LiH的电子式为 。核外有2个电子的简单阴、阳离子有若干种,试比较它们半径的大小 。
25.非金属元素R的气态氢化物的化学式为H8-nR,则R的最高氧化物的化学式为 。
26.根据下表中的键能数据,写出氮气、氢气合成氨气的热化学方程式 。在合成氨的工业生产中,科学家在努力寻找活性温度更低的新催化剂,简述其意义 。
共价键 | 键能(KJ/ mol) |
N≡N | 946 |
H-H | 436 |
H-N | 391 |
27.钯(Pd)是优良的储氢金属:2Pd (s)+xH2(g) 2PdHx (s)?H=-Q(Q>0)
2PdHx (s)?H=-Q(Q>0)
通常状况下,x的最大值为0.8,为使x>0.8可采取的措施是 ;为使PdHx 产生H原子并在固体中快速流动,可采取的措施是 (选填编号)。
A.升温 B.减压 C.及时移走金属钯
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市静安区高三上学期期末考试化学试卷(解析版) 题型:选择题
以下反应不属于“同一价态的同种元素既被氧化又被还原”的是
A.硫代硫酸钠与稀硫酸 B.硫与热NaOH溶液
C. H2O2溶液中加入MnO2 D.KClO3与盐酸
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省滕州市高三12月月考理综化学试卷(解析版) 题型:选择题
某离子反应涉及H2O、ClO—、IO3—、OH—、I2、Cl—六种微粒。其中c(ClO—)随反应进行逐渐减小。下列判断错误的是
A.该反应的还原剂是I2
B.氧化剂与还原剂的物质的量之比为5:2
C.消耗1 mol氧化剂,转移2 mol电子
D.反应后溶液的碱性明显减弱
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com