
| ||


 小学期末标准试卷系列答案
小学期末标准试卷系列答案科目:高中化学 来源:2010-2011学年上海市闸北区高三上学期期末考试化学试卷 题型:计算题
.某校实验员将一定量的KClO3与若干MnO2混合,由于MnO2含量过少, KClO3与MnO2不能充分接触,加热后① KClO3分解生成KCl和O2 ;②4KClO3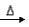 3KClO4+KCl
。上述两个反应同时发生。
3KClO4+KCl
。上述两个反应同时发生。
(1)若取用的KClO3为98.0克,放置在试管中加热至质量不再变化时,得到的KClO4的质量为27.7克,则收集到标准状况下的O2多少升?
(2)若使98.0克KClO3在一定条件下完全分解可生成KCl的物质的量为多少?
(3)若取用的KClO3为73.5克,放置在试管中加热,当生成0.25摩尔KCl和6.72升标准状况的O2时停止加热,则该反应中KClO3的分解率为多少?
(4)若取用的KClO3为122.5 克,在一定条件下完全反应分解生成x摩尔KCl和y摩尔O2,试建立y和x之间的函数关系。
查看答案和解析>>
科目:高中化学 来源:2011-2012年浙江省高一上学期期中考试化学试卷 题型:选择题
将0.2摩MnO2和50毫升12mol/L盐酸混合后缓缓加热,反应完全后向留下的溶液中加入足量AgNO3溶液,生成AgCl沉淀物质的量为(不考虑盐酸的挥发)
A.等于0.3摩 B.小于0.3摩
C.大于0.3摩,小于0.6摩 D.以上结论都不正确
查看答案和解析>>
科目:高中化学 来源: 题型:
将0.2摩MnO2和50毫升12mol/L盐酸混合后缓缓加热,反应完全后向留下的溶液中加入足量AgNO3溶液,生成AgCl沉淀物质的量为(不考虑盐酸的挥发)
A.等于0.3摩 B.小于0.3摩
C.大于0.3摩,小于0.6摩 D.以上结论都不正确
查看答案和解析>>
科目:高中化学 来源:2011-2012年浙江省绍兴一中高一上学期期中考试化学试卷 题型:单选题
将0.2摩MnO2和50毫升12mol/L盐酸混合后缓缓加热,反应完全后向留下的溶液中加入足量AgNO3溶液,生成AgCl沉淀物质的量为(不考虑盐酸的挥发)
| A.等于0.3摩 | B.小于0.3摩 |
| C.大于0.3摩,小于0.6摩 | D.以上结论都不正确 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com